网址:http://m.1010jiajiao.com/timu3_id_8389[举报]
(1)常压的条件下,向氮化硅中添加氧化铝,经高温烧结可制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料“赛伦”,化学式可表示为Si6-xAlxOxN8-x.不同温度下x的值不同,在1400℃时x为2.0,则“赛伦”,中氮元素的化合价为
(2)炒菜的油锅着火,相信你能采取两种不同的原理灭火.你的灭火方法是
(3)去年入秋以来,西南地区特别是云南遭受了百年一遇的特大干旱.气象专家分析认为,全球气候变暖,太平洋厄尔尼诺现象加剧,破坏了大气结构,造成海洋季风无法登陆形成降雨,是导致这次极端干旱的主要原因.世界各国已经意识到温室效应的严重性.2009年12月7~19日,联合国气候大会在丹麦首都哥本哈根召开,达成了一项无减排目标和约束力的《哥本哈根协议》,减排指的是减少二氧化碳的排放量.“低碳”已成为我们的共识.请回答下列问题:
①为解决温室效应加剧,科学家正在研究如下图所示的二氧化碳新的循环体系.
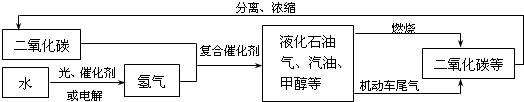
从图中分析得出的下列结论中,正确的是
A.二氧化碳也是一种重要的资源
B.分离、浓缩得到二氧化碳是化学变化
C.无机物和有机物可以相互转化
D.液化石油气、汽油、甲醇等物质中共含有碳、氢、氧三种元素
E.化学能可以转化为热能、光能、机械能等,光能或电能也可以转化为化学能
②2010年世博会5月1日在我国上海开幕.下列设计或活动能体现“低碳”理念的是
A.用牛奶等废弃饮料纸包装制成环保椅、环保垃圾桶和节目册等参观者服务设施
B.利用老厂房进行改造成宝钢大舞台、船坞等重要演出场地
C.世界自然基金会(WWF)将于6月5日举办音乐会,演出过程中还将“熄灯一小时”,这一小时演出舞美所需电力均由太阳能蓄电池供电.
D.中国国家馆所有的门窗都采用LOM-E玻璃,将阳光转化为电能并储存起来,为建筑外墙照明提供能量
E.超过1000辆的新能源汽车服务于世博
③“低碳”生活、人人有责.如果你想利用暑假去上海参加世博会,请你在交通、餐饮、生活等方面提出两条符合“低碳”理念的做法:
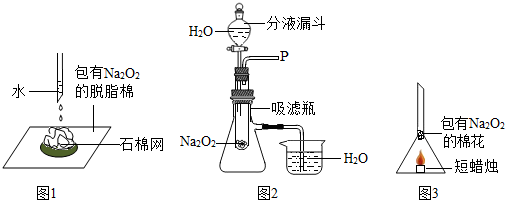
提出猜想:
a)小新认为过氧化钠(Na2O2)与水反应生成了可以支持燃烧的物质.
b)小海又根据燃烧的条件,对小新的猜想进行了补充
实验与分析:同学们设计了如图2的实验装置.
(1)打开分液漏斗的活塞,控制水滴加的速度,看到试管中有气泡产生,将带火星的木条靠近P出口,看到木条复燃,你推测此气体可能是
(2)实验中还观察到,烧杯中的导气管口有气泡冒出,产生这一现象的原因是
(3)完成了以上实验,同学们又展开了进一步的研究,继续探究反应后生成的另一种物质是什么?小新猜想另一种物质是Na2CO3,小海认为不可能,小海的依据是
老师介绍:
a)过氧化钠和水发生反应生成氧气和氢氧化钠.
b)过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气,因而,经常被用于潜水艇和防毒面具中提供氧气.
补充实验:
确定了以上性质,小海同学又设计了一个实验(如图3)将一团包有过氧化钠的粉末的棉花塞到漏斗的管中,漏斗下方点燃一支短蜡烛 (蜡烛火焰与棉花不接触),棉花会燃烧起来吗?简要说明理由
反思:结合上述实验事实,同学们对于运输过氧化钠固体提出了安全建议:
碱石灰是氧化钙和氢氧化钠的固体混合物,是实验室常用的干燥剂。相关信息如下图所示。同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究。

[提出问题]实验室中久置的碱石灰样品的成分是什么?
[进行猜想] 久置的碱石灰样品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分。用化学方程式表示样品中含有Ca(OH)2或Na2CO3可能含有的原因 (写一个)
[探究过程]

试回答下列问题:
(1)操作①的名称是 ,溶液C中一定含 离子。
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有 ,反应的方程式为 。
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是 。
[实验结论]
依据上述实验操作过程及现象,综合对滤液和固体成分的探究,下列对样品成分的分析正确的是 (填序号)
①样品中一定含NaOH ②样品中一定含Na2CO3 ③样品中含NaOH、CaO中的一种或两种
[拓展延伸]
为测定实验室中一瓶变质的烧碱中NaOH的含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g。请分析计算:
(1)反应产生的CO2的质量为 g。
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是多少?(写出计算过程)
(3)用同浓度的硫酸,分别与未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等。从钠元素质量守恒的角度解释其原因是: 。
【解析】[进行猜想]生成氢氧化钙的方程式为CaO+H2O═Ca(OH)2 生成碳酸钠的方程式为2NaOH+CO2═Na2CO3+H2O
[探究过程]
(1)将固液分离的操作为过滤,酚酞变红了,说明溶液显碱性,故溶液中一定含有OH—
(2)能与氯化钙反应的是碳酸钠,其反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓
(3)可以取溶液C于试管中滴加碳酸钠溶液,有白色沉淀生成,则说明CaCl2溶液已过量
[实验结论]因为加水后烧杯壁变热说明样品中含有氢氧化钠或者是氧化钙,或者是二者都有,加入氯化钙生成白色沉淀说明样品中一定含有碳酸钠,综合以上分析,故选②③
[拓展延伸]
(1)根据质量守恒定律可求出反应产生的CO2的质量为200g+200g-395.6g=4.4g
(2)根据二氧化碳的质量为4.4克就可以计算了,根据化学反应方程式计算,即可得出样品中碳酸钠的质量,继而得出原样品中氢氧化钠的质量,具体步骤见答案。
(3)氢氧化钠和碳酸钠都是每46g钠元素生成142g硫酸钠,消耗98g硫酸
查看习题详情和答案>>
碱石灰是氧化钙和氢氧化钠的固体混合物,是实验室常用的干燥剂。相关信息如下图所示。同学们为确认一瓶久置的“碱石灰”(可能已部分变质或全部变质)样品的成分,进行如下探究。

[提出问题]实验室中久置的碱石灰样品的成分是什么?
[进行猜想] 久置的碱石灰样品中可能含有CaO、NaOH、Na2CO3、Ca(OH)2、CaCO3等成分。用化学方程式表示样品中含有Ca(OH)2或Na2CO3可能含有的原因 (写一个)
[探究过程]

试回答下列问题:
(1)操作①的名称是 ,溶液C中一定含 离子。
(2)溶液A中加入CaCl2溶液后产生固体,说明样品中一定含有 ,反应的方程式为 。
(3)向溶液A中加入CaCl2溶液后,证明CaCl2溶液过量的方法是 。
[实验结论]
依据上述实验操作过程及现象,综合对滤液和固体成分的探究,下列对样品成分的分析正确的是 (填序号)
①样品中一定含NaOH ②样品中一定含Na2CO3 ③样品中含NaOH、CaO中的一种或两种
[拓展延伸]
为测定实验室中一瓶变质的烧碱中NaOH的含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g。请分析计算:
(1)反应产生的CO2的质量为 g。
(2)若所取烧碱样品为50.0g,则样品中NaOH的质量分数是多少?(写出计算过程)
(3)用同浓度的硫酸,分别与未变质、部分变质、或全部变质(杂质都是Na2CO3)的烧碱样品反应,需要硫酸的质量都相等。从钠元素质量守恒的角度解释其原因是: 。
【解析】[进行猜想]生成氢氧化钙的方程式为CaO+H2O═Ca(OH)2 生成碳酸钠的方程式为2NaOH+CO2═Na2CO3+H2O
[探究过程]
(1)将固液分离的操作为过滤,酚酞变红了,说明溶液显碱性,故溶液中一定含有OH—
(2)能与氯化钙反应的是碳酸钠,其反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓
(3)可以取溶液C于试管中滴加碳酸钠溶液,有白色沉淀生成,则说明CaCl2溶液已过量
[实验结论]因为加水后烧杯壁变热说明样品中含有氢氧化钠或者是氧化钙,或者是二者都有,加入氯化钙生成白色沉淀说明样品中一定含有碳酸钠,综合以上分析,故选②③
[拓展延伸]
(1)根据质量守恒定律可求出反应产生的CO2的质量为200g+200g-395.6g=4.4g
(2)根据二氧化碳的质量为4.4克就可以计算了,根据化学反应方程式计算,即可得出样品中碳酸钠的质量,继而得出原样品中氢氧化钠的质量,具体步骤见答案。
(3)氢氧化钠和碳酸钠都是每46g钠元素生成142g硫酸钠,消耗98g硫酸
查看习题详情和答案>>
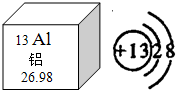 铝被称为“年轻的金属”,据世界化学史记载,金属铝是在1825年才被英国化学家戴维制得.今天,铝已经进入了我们生活的每一个角落.
铝被称为“年轻的金属”,据世界化学史记载,金属铝是在1825年才被英国化学家戴维制得.今天,铝已经进入了我们生活的每一个角落.(1)①铝在地壳中的含量居所有金属元素的第
A.铝原子 B.铝离子 C.铝分子
②工业上用电解氧化铝制取金属铝,同时生成一种常见的气体.反应的方程式为
| ||
| ||
③工业上从铝土矿中获得氧化物X,从空气中获得氮气,再将物质X、N2和碳在一定条件下反应制得AlN和CO.化学反应方程式为
| ||
| ||
(2)铝合金比单质铝有着更为广泛的应用.已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
[查阅资料]铝与氢氧化钠溶液反应方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
[猜 想]猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有
猜想3:该合金粉末中除铝外,还含有铁、铜.
[实验探究]下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%NaOH溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有 铝 铝 . |
| ②取步骤①所得滤渣,加过量的 10%盐酸 10%盐酸 ,充分反应. |
滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有 铁和铜 铁和铜 . |
[反 思]一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.等质量铝与足量盐酸反应生成的氢气比其与足量氢氧化钠溶液生成的氢气
A.多 B.少 C.相等 D.无法比较
(3)在烧杯中加入4.28g久置空气中的铝箔,再滴加稀盐酸,放出气体的质量与所加稀盐酸质量的关系如右图所示.请回答下列问题:
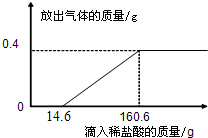
①产生氢气
②刚开始没有氢气放出的原因是铝箔表面有
③所滴加的稀盐酸中溶质的质量分数.