摘要:6.已知25℃时.电离常数Ka(HF)=3.6×10-4 mol/L.溶度积常数Ksp(CaF2)=1.46×10-10.现向1 L 0.2 mol/L HF溶液中加入1 L 0.2 mol/L CaCl2溶液.则下列说法不正确的是 ( ) A.25℃时.0.1 mol/L HF溶液中pH>1 B.Ksp(CaF2)随温度的变化而变化 C.氟化钙和氟化氢都是弱电解质 D.该体系中有CaF2沉淀产生 解析:因为HF是弱电解质.所以0.1 mol/L HF溶液中pH>1.氟化钙是难溶的强电解质.故C项符合题意. 答案:C
网址:http://m.1010jiajiao.com/timu3_id_83630[举报]
已知25℃时,电离常数Ka(HF)=3.6×10-4mol?L-1,溶度积常数KSP(CaF2)=1.46×10-10 mol3?L-3.现向1L 0.2mol?L-1HF溶液中加入1L 0.2mol?L-1CaCl2溶液,则下列说法中正确的是( )
查看习题详情和答案>>
已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10.现向1L0.2mol?L-1HF溶液中加入1L0.2mol?L-1CaCl2溶液,则下列说法中正确的是( )
(2008?龙湖区模拟)已知25℃时,电离常数Ka(HF)=3.6×10-4 mol?L-1,溶度积常数Ksp(CaF2)=1.46×10-10mol3?L-3.现向1L0.2mol?L-1HF溶液中加入1L0.2mol?L-1CaCl2溶液,则下列说法中,正确的是( )
(2011?青岛模拟)已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10.现向1L 0.2mol?L-1HF溶液中加入1L 0.2mol?L-1CaCl2溶液,则下列说法中,正确的是( )
查看习题详情和答案>>
(1)(4分)高炉炼铁过程中发生的主要反应为:1/3Fe2O3(s)+CO(g)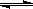 2/3Fe (s)+CO2(g),已知该反应在不同温度下的平衡常数如下。则:
2/3Fe (s)+CO2(g),已知该反应在不同温度下的平衡常数如下。则:
①该反应的△H_____0(填“>”、“<”或“=”);
②在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡。求CO的平衡转化率= ________。
(2)(3分)常温下,HR(酸)溶液pH=3,MOH(碱)的溶液pH=11,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式
___________________________________________。
(3)(3分)25℃时,pH=0的HCl、0.1mol/L的HCl、0.01mol/L的NaOH、pH=14的NaOH四种溶液中由水电离产生的c(H+)之比为 。
(4)(3分)已知25℃时,电离常数Ka(HF)=3.6×10-4,则0.1 mol·L-1 HF溶液中c(H+)= mol·L-1。