摘要:3.m g Na与足量Cl2反应.生成固体的质量为(m+3.55) g.则等量Na与O2反应.生成固体的质量可能为 ( ) ①(m+0.8)g ②(m+1.1) g ③(m+1.4) g ④(m+1.6) g A.① B.④ C.②③ D.都有可能 解析:钠与Cl2反应生成NaCl.由此可知钠为0.1 mol.而Na与O2反应可以生成Na2O或Na2O2.则此增加的质量介于0.8 g和1.6 g之间.最后生成的固体质量都有可能.选D. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_83495[举报]
m g Na与足量Cl2反应,生成固体的质量为(m+3.55) g,则等量Na与O2反应,生成固体的质量可能为
[ ]
①(m+0.8)g ②(m+1.1) g ③(m+1.4) g ④(m+1.6) g
A.①
B.④
C.②③
D.都有可能
查看习题详情和答案>>
A.①
B.④
C.②③
D.都有可能
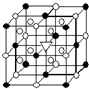 A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子
A.(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞.图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽图中●、○中的一种.图中●、○分别指代哪种粒子AlF6-
AlF6-
、Na+
Na+
;大立方体的体心处▽所代表的是AlF6-
AlF6-
.冰晶石在化工生产中的用途电解炼铝的助熔剂
电解炼铝的助熔剂
.(2)H2S和H2O2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
H2O2分子间存在氢键,与水分子可形成氢键
H2O2分子间存在氢键,与水分子可形成氢键
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.写出铜原子价电子层的电子排布式
3d104s1
3d104s1
,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有Cr
Cr
(填元素符号).实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有共价键和配位键
共价键和配位键
.实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4?H2O晶体.实验中所加C2H5OH的作用是降低Cu(NH3)4SO4?H2O的溶解度
降低Cu(NH3)4SO4?H2O的溶解度
.B.用含少量铁的氧化铜制取氯化铜晶体(CuCl2?xH2O).有如下操作:
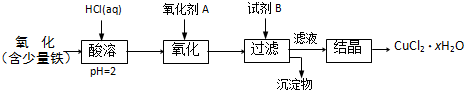
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解.
(1)加热酸溶过程中发生反应的离子方程式有:
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
Fe+2H+=Fe2++H2↑、CuO+2H+=Cu2++H2O
(2)氧化剂A可选用
①
①
(填编号,下同)①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用
③
③
①NaOH ②FeO ③CuO
(4)试剂B的作用是
①③
①③
①提高溶液的pH ②降低溶液的pH ③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是
②④①
②④①
(按实验先后顺序填编号)①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g.
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g.
试评价上述两种实验方案,其中正确的方案是
二
二
,据此计算得x=| 80m-135n |
| 18n |
| 80m-135n |
| 18n |