摘要:9.Na3N与NaH均为离子化合物.都能与水反应放出气体.下列有关叙述不正确的是 ( ) A.二者中Na+半径都比阴离子大 B.与水反应时.水的作用不同 C.与水反应所得溶液均能使酚酞试液变红 D.二者与盐酸反应.前者可产生两种盐.后者只有一种盐生成 解析:Na+的离子结构示意图为.N3-的离子结构示意图为 .H-的离子结构示意图为.所以离子半径为N3->Na+>H-.A错误,Na3N与水反应的化学方程式为:Na3N+3H2O===3NaOH+NH3↑.NaH与H2O发生反应的化学方程式为:NaH+H2O===NaOH+H2↑.前者是水解反应.后者是氧化还原反应.其中NaH是还原剂.水是氧化剂.故B正确,因均有NaOH生成.所以均能使酚酞变红.C正确,D项中.前者生成NaCl与NH4Cl两种盐.后者只生成NaCl一种. 答案:A
网址:http://m.1010jiajiao.com/timu3_id_83487[举报]
Na3N与NaH均为离子化合物,都能与水反应放出气体.下列有关叙述不 正确的是( )
A.二者中Na+半径都比阴离子大
B.与水反应时,水的作用不同
C.与水反应所得溶液均能使酚酞试液变红
D.二者与盐酸反应,前者可产生两种盐,后者只有一种盐生成
查看习题详情和答案>>
A.二者中Na+半径都比阴离子大
B.与水反应时,水的作用不同
C.与水反应所得溶液均能使酚酞试液变红
D.二者与盐酸反应,前者可产生两种盐,后者只有一种盐生成
查看习题详情和答案>>
Na3N与NaH均为离子化合物,都能与水反应放出气体.下列有关叙述不 正确的是
- A.二者中Na+半径都比阴离子大
- B.与水反应时,水的作用不同
- C.与水反应所得溶液均能使酚酞试液变红
- D.二者与盐酸反应,前者可产生两种盐,后者只有一种盐生成
Na3N与NaH均为离子化合物,都能与水反应放出气体.下列有关叙述不正确的是
[ ]
A.二者中Na+半径都比阴离子大
B.与水反应时,水的作用不同
C.与水反应所得溶液均能使酚酞试液变红
D.二者与盐酸反应,前者可产生两种盐,后者只有一种盐生成
查看习题详情和答案>>
B.与水反应时,水的作用不同
C.与水反应所得溶液均能使酚酞试液变红
D.二者与盐酸反应,前者可产生两种盐,后者只有一种盐生成
(A)海底热液研究处于当今科研的前沿.海底热液活动区域“黑烟囱”的周围,存活的长管虫、蠕虫、蛤类、贻贝类等动植物,成了极佳的天然海底实验室,且海底“黑烟囱”周围常存在FeS、黄铜矿及锌矿等矿物.
(1)有关几种气体分子的说法正确的是 .
A.CO的结构式可表示为
B.CO2与COS(硫化羰)互为等电子体
C.NH3分子中氮原子采用sp2杂化
D.HCN分子呈直线形
(2)酸性热液中大量存在一价阳离子,结构如图2,它的化学式为: .
(3)铁原子核外电子排布式为: .
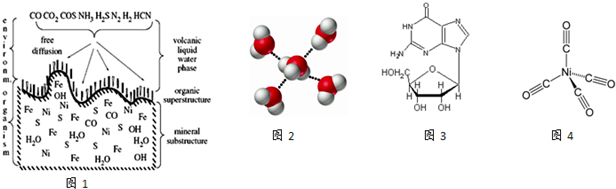
(4)“黑烟囱“热液冷却后若可检测出图3所示分子,该分子中手性碳原子数为: .
(5)FeS与NaCl均为离子晶体,晶胞相似,前者熔点为985℃,后者801℃,其原因是 .
(6)从“黑烟囱“形成的矿床中提取镍,需将其转化为四羰基合镍(结构如图4),则该络合物的配位数为 .
查看习题详情和答案>>
(1)有关几种气体分子的说法正确的是
A.CO的结构式可表示为

B.CO2与COS(硫化羰)互为等电子体
C.NH3分子中氮原子采用sp2杂化
D.HCN分子呈直线形
(2)酸性热液中大量存在一价阳离子,结构如图2,它的化学式为:
(3)铁原子核外电子排布式为:

(4)“黑烟囱“热液冷却后若可检测出图3所示分子,该分子中手性碳原子数为:
(5)FeS与NaCl均为离子晶体,晶胞相似,前者熔点为985℃,后者801℃,其原因是
(6)从“黑烟囱“形成的矿床中提取镍,需将其转化为四羰基合镍(结构如图4),则该络合物的配位数为