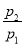摘要:4.充分燃烧一定量的丁烷生成CO2和液态水.放热Q kJ.经测定生成的CO2恰好被100 mL 5mol/L的KOH溶液吸收生成K2CO3.则热化学方程式:C4H10(g)+6.5O2(g)===4CO2(g)+5H2O(l)的ΔH为 ( ) A.-16Q kJ/mol B.+16 Q kJ/mol C.-8Q kJ/mol D.+8Q kJ/mol 解析:先求CO2的物质的量.由2KOH+CO2===K2CO3+H2O知n(CO2)=n(KOH)=×0.1 L×5 mol/L=0.25 mol.由生成0.25 mol CO2放热Q kJ.可知 1 mol C4H10完全燃烧生成 4 mol CO2放热 16Q kJ.因为是放热反应.故ΔH=-16 Q kJ/mol. 答案:A
网址:http://m.1010jiajiao.com/timu3_id_83110[举报]
充分燃烧一定量的丁烷生成CO2和液态水,放热Q kJ.经测定生成的CO2恰好被100 mL 5mol/L的KOH溶液吸收生成K2CO3,则热化学方程式:C4H10(g)+6.5O2(g)===4CO2(g)+5H2O(l)的ΔH为
[ ]
A.-16Q kJ/mol
B.+16 Q kJ/mol
C.-8Q kJ/mol
D.+8Q kJ/mol
查看习题详情和答案>>
B.+16 Q kJ/mol
C.-8Q kJ/mol
D.+8Q kJ/mol
充分燃烧一定量丁烷生成CO2和液态水放热Q kJ,经测定生成的CO2恰好被100mL 5mol/L的KOH溶液完全吸收生成K2CO3,则热化学方程式:C4H10(g)+
O2(g)═4CO2(g)+5H2O(l)的△H为( )
| 13 |
| 2 |
| A、+8Q kJ?mol-1 |
| B、-8Q kJ?mol-1 |
| C、-16Q kJ?mol-1 |
| D、+16Q kJ?mol-1 |
在室温下,向某一容积固定的真空容器内充入丁烷(气)和氧气,使容器内混合气的总压强达到P1,点火燃烧,丁烷和氧气恰好都完全反应,冷却至室温后,容器内气体的总压强为P2.(以下计算结果保留两位有效数字)
(1)若丁烷燃烧的生成物只有H2O(液)和CO2,则 =________.
=________.
(2)若 =0.64,求反应后容器内所含各物质的物质的量之比和反应前混合气中丁烷的物质的量分数.
=0.64,求反应后容器内所含各物质的物质的量之比和反应前混合气中丁烷的物质的量分数.
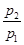 =0.64,则反应前混合气中丁烷的物质的量分数= 。
=0.64,则反应前混合气中丁烷的物质的量分数= 。