摘要:13.下图为某市售盐酸试剂瓶标签上的部分数据.问: (1)该盐酸的物质的量浓度为多少? (2)取该盐酸25.5 mL与2.00 mol/L的氢氧化钠溶液100 mL混合.再将混合后溶液稀释至1.00 L.此时溶液的pH约为多少? 解析:(1)c(HCl)= =11.8 mol/L. (2)n(HCl)=11.8 mol/L×0.0255 L≈0.300 mol. n=2.00 mol/L×0.100 L=0.200 mol. 混合并稀释后溶液中 c(H+)==0.100 mol/L. pH=-lgc(H+)=1. 答案:(1)c(HCl)==11.8 mol/L (2)1
网址:http://m.1010jiajiao.com/timu3_id_82979[举报]
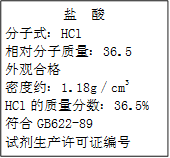
下图为某市售盐酸试剂瓶标签上的部分数据。问:
| 盐 酸 分子式:HCl 相对分子质量:36.5 外观合格 密度约:1.18 g/cm3 HCl的质量分数:36.5% 符合GB622~89 试剂生产许可证编号: |
(1)该盐酸的物质的量浓度为多少?(列式计算)
(2)取该盐酸25.5 mL与2.00 mol/L的氢氧化钠溶液100 mL混合,再将混合后溶液稀释至1.00 L,此时溶液的pH约为多少?
查看习题详情和答案>>(5分)下图为某市售盐酸试剂瓶标签上的部分数据。问:

(1)该盐酸的物质的量浓度为多少?
(2)取该盐酸25.4 mL与2.00 mol·L-1的氢氧化钠
溶液100 mL混合,再将混合液稀释到1.00 L,
此时溶液的pH约为多少?
查看习题详情和答案>>
下图为某市售盐酸试剂瓶标签上的部分数据。问:
盐 酸 分子式:HCl 相对分子质量:36.5 外观合格 密度约: HCl的质量分数:36.5% 符合GB622-89 试剂生产许可证编号: |
(1)该盐酸的物质的量浓度为多少?(列式计算)
(2)取该盐酸25.4 mL与2.00 mol·L-1的氢氧化钠溶液100 mL混合,再将混合后溶液稀释至