摘要:7.碳化硅这种结构类似于金刚石的晶体.其中碳原子和硅原子的位置是交替的.在下列三种晶体①金刚石,②晶体硅,③碳化硅中.它们的熔点从高到低的顺序是 ( ) A.①③② B.②③① C.③①② D.②①③ 答案: 7.A 熔点高低取决于共价键强弱.共价键强弱又与各原子的原子半径有关.C的原子半径小于Si的原子半径
网址:http://m.1010jiajiao.com/timu3_id_82610[举报]
FeS2结构类似于Na2O2,与酸反应时生成H2S2,H2S2类似于H2O2,易分解.实验室用稀盐酸制取H2S时,某学生误将FeS2颗粒当作FeS使用,当FeS2反应完后,不可能生成的物质是( )
查看习题详情和答案>>
FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时生成H2S2,H2S2易分解.实验室用稀硫酸与FeS2颗粒混合,则反应完毕后不可能生成的物质是( )
| A、H2S | B、S | C、FeS | D、FeSO4 |
(2010?山东)碳族元素包括C、Si、Ge、Sn、Pb.
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(3)用价层电子对互斥理论推断SnBr2分子中Sn-Br键的键角
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心.该化合物化学式为
查看习题详情和答案>>
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过
SP2
SP2
杂化与周围碳原子成键,多层碳纳米管的层与层之间靠范德华力
范德华力
结合在一起.(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
C>H>Si
C>H>Si
.(3)用价层电子对互斥理论推断SnBr2分子中Sn-Br键的键角
<
<
120°(填“>”“<”或“=”)(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心.该化合物化学式为
PbBaO3
PbBaO3
,每个Ba2+与12
12
个O2-配位.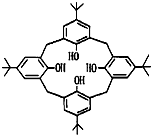 杯环芳烃因其结构类似于酒杯而得名,其键线式如图,下列关于杯环芳烃的说法正确的是( )
杯环芳烃因其结构类似于酒杯而得名,其键线式如图,下列关于杯环芳烃的说法正确的是( )| A、属于芳香烃 | B、最多与6mol H2发生加成反应 | C、分子式为C44H56O4 | D、分子内所有原子一定在同一平面上 |
| |||||||||||||||||||