摘要:25.含FeS280%的硫铁矿燃烧时损失硫5%.用SO2氧化成SO2时利用率为99%.问生产l t98%的硫酸需这种硫铁矿多少吨? 答案:25.解:设需80%的FeS2为xt x=0.797t
网址:http://m.1010jiajiao.com/timu3_id_82335[举报]
工业上制硫酸的主要反应如下:4FeS2+11O2═2Fe2O3+8SO2; 2SO2+O2
2SO3; SO3+H2O═H2SO4用含FeS280%的硫铁矿生成硫酸,已知该矿石的利用率为95%,SO2的转化率为90%,SO3的吸收过程中损失率为2%.求生产500t98%的硫酸需矿石的质量.(要写出简单计算过程)
查看习题详情和答案>>
| ||
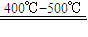 2SO3; SO3+H2O═H2SO4用含FeS280%的硫铁矿生成硫酸,已知该矿石的利用率为95%,SO2的转化率为90%,SO3的吸收过程中损失率为2%.求生产500t98%的硫酸需矿石的质量.(要写出简单计算过程)
2SO3; SO3+H2O═H2SO4用含FeS280%的硫铁矿生成硫酸,已知该矿石的利用率为95%,SO2的转化率为90%,SO3的吸收过程中损失率为2%.求生产500t98%的硫酸需矿石的质量.(要写出简单计算过程)