摘要:3.(2010·陕西师大附中1月考题)在一定条件下.科学家利用从烟道气中分离出的CO2 与太阳能电池电解水产生的H2合成甲醇.已知CH3OH.H2的燃烧热分别为:ΔH1 =-725.5 kJ/mol.ΔH2=-285.8 kJ/mol.合成过程如下图所示.下列说法不正确的是( ) A.“阳光→电池→光电池→电解水 过程中的能量变化是光能→电能→化学能 B.该合成路线对于环境保护的价值是有利于防止温室效应 C.乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性.其原因可表示为:HOCH2CH2NH2+H2OHOCH2CH2NH3++OH- D.以CO2.H2合成CH3OH的热化学方程式为:CO2(g)+3H2(g)===CH3OH(l)+H2O(l),ΔH=+131.9 kJ/mol 解析:A项正确,该过程中能将CO2吸收再利用.B项正确,胺与NH3类似.水溶液呈弱碱性.C项正确,ΔH=反应物燃烧热总和-生成物燃烧热总和=0++0=-131.9[注意CO2(g).H2O(l)都为稳定的氧化物.燃烧热都为0].D项不正确. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_81648[举报]
Ⅰ.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如图所示,试回答下列问题:
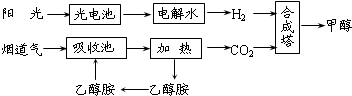
(1)该合成路线对于环境保护的价值在于 .
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因 .
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: .
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g)+6H2(g)
CH3OCH3(g)+3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
(4)该反应的焓变△H 0,熵变△S 0(填>、<或=).
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 .若以1.12L?min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9℃),用该电池电解500mL 2mol?L-1CuSO4溶液,通电0.50min后,理论上可析出金属铜 g.
查看习题详情和答案>>

(1)该合成路线对于环境保护的价值在于
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g)+6H2(g)
| 催化剂 |
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2)/n(CO2)] | 500K | 600K | 700K | 800K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式
(1)将CO2转化成有机物可有效实现碳循环.如:
①6CO2+6H2O
C6H12O6+6O2
②CO2+CH4
CH3COOH
③2CO2+6H2
CH2=CH2+4H2O
对以上反应的叙述,正确的是
A.最节能的是反应①
B.反应②的原子利用率为100%
C.反应②中的两种反应物都是可再生的天然物质
D.反应③是目前工业生产乙烯的最主要方法
(2)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如图所示,试回答下列问题:
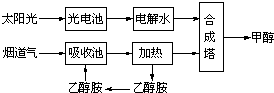
①15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性(与NH3溶于水的原理相似),上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
②CH3OH(l)、H2(g)的燃烧热分别为:△H=-725.5kJ?mol-1、△H=-285.8kJ?mol-1,写出工业上以CO2(g)、H2(g)合成CH3OH(l)的热化学方程式:
③据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇也已成为现实:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),该反应的△S
查看习题详情和答案>>
①6CO2+6H2O
| 光合作用 |
②CO2+CH4
| 催化剂 |
| △ |
③2CO2+6H2
| 催化剂 |
| △ |
对以上反应的叙述,正确的是
AB
AB
.(填序号)A.最节能的是反应①
B.反应②的原子利用率为100%
C.反应②中的两种反应物都是可再生的天然物质
D.反应③是目前工业生产乙烯的最主要方法
(2)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如图所示,试回答下列问题:

①15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性(与NH3溶于水的原理相似),上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-
HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-
.②CH3OH(l)、H2(g)的燃烧热分别为:△H=-725.5kJ?mol-1、△H=-285.8kJ?mol-1,写出工业上以CO2(g)、H2(g)合成CH3OH(l)的热化学方程式:
CO2(g)+3H2(g)═CH3OH(l)+H2O(l),△H=-131.9KJ/mol
CO2(g)+3H2(g)═CH3OH(l)+H2O(l),△H=-131.9KJ/mol
.③据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇也已成为现实:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),该反应的△S
<
<
(填“>”、“=”或“<”)0,根据反应可自发进行,推得该反应的△H<
<
(填“>”、“=”或“<”)0.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如图所示,试回答下列问题:

(1)该合成路线对于环境保护的价值在于
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
(3)CH3OH(l)、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
(4)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇也已成为现实.
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)下列叙述正确的是
a.使用Cu-Zn-Fe催化剂可大大提高生产效率
b.反应需在300℃进行可推测该反应是吸热反应
c.充入大量CO2气体可提高H2的转化率
d.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率.
查看习题详情和答案>>

(1)该合成路线对于环境保护的价值在于
有利于防止温室效应
有利于防止温室效应
.(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-
HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-
.(3)CH3OH(l)、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
CO2(g)+3H2(g)→CH3OH(l)+H2O(l)△H=-131.9kJ/mol
CO2(g)+3H2(g)→CH3OH(l)+H2O(l)△H=-131.9kJ/mol
.(4)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇也已成为现实.
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)下列叙述正确的是
acd
acd
.a.使用Cu-Zn-Fe催化剂可大大提高生产效率
b.反应需在300℃进行可推测该反应是吸热反应
c.充入大量CO2气体可提高H2的转化率
d.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率.
在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:
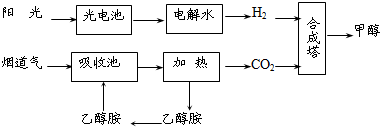
(1)该合成路线对于环境保护的价值在于 ;
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因: ;
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: ;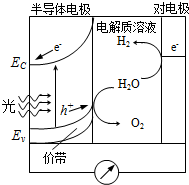
(4)科学家发明了一种基于如图所示原理的廉价光电化学电池装置,写出光照时半导体电极表面发生的电极反应式 .目前应用最多的半导体材料是Si,甚至有人提出硅是“21世纪的能源”,硅可作为新能源的原因可能的是 .
a.在自然界中存在大量的单质硅
b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多
d.硅的化学性质不活泼,便于安全运输、贮存.
查看习题详情和答案>>

(1)该合成路线对于环境保护的价值在于
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:

(4)科学家发明了一种基于如图所示原理的廉价光电化学电池装置,写出光照时半导体电极表面发生的电极反应式
a.在自然界中存在大量的单质硅
b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多
d.硅的化学性质不活泼,便于安全运输、贮存.
(14分)Ⅰ.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:

(1)该合成路线对于环境保护的价值在于 。
(2)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因 。
(3)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: 。
Ⅱ.将燃煤废气中的CO2转化为甲醚的反应原理为:
2CO2(g) + 6H2(g) CH3OCH3(g)
+ 3H2O(g)
CH3OCH3(g)
+ 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
|
投料比[n(H2) / n(CO2)] |
500 K |
600 K |
700 K |
800 K |
|
1.5 |
45% |
33% |
20% |
12% |
|
2.0 |
60% |
43% |
28% |
15% |
|
3.0 |
83% |
62% |
37% |
22% |
(4)该反应的焓变△H 0,熵变△S___0(填>、<或=)。
(5)用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜 g。
查看习题详情和答案>>