摘要:3.在一定浓度的FeCl3溶液中.存在如下水解平衡:Fe3++3H2O Fe(OH)3+3H+. 在此溶液中滴入饱和的FeCl3溶液.下列说法中正确的是 ( ) A.水解平衡向正反应方向移动 B.水解平衡向逆反应方向移动 C.溶液中H+浓度不变 D.Fe3+的水解程度增大 解析:增加Fe3+浓度.水解平衡向正方向移动.达到平衡后溶液中H+浓度增大. 但Fe3+的水解百分率减小. 答案:A
网址:http://m.1010jiajiao.com/timu3_id_81481[举报]
在一定浓度的FeCl3溶液中,存在如下水解平衡:Fe3++3H2O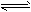 Fe(OH)3+3H+,在此溶液中滴入饱和的FeCl3溶液,下列哪个变化的说法正确
Fe(OH)3+3H+,在此溶液中滴入饱和的FeCl3溶液,下列哪个变化的说法正确
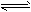 Fe(OH)3+3H+,在此溶液中滴入饱和的FeCl3溶液,下列哪个变化的说法正确
Fe(OH)3+3H+,在此溶液中滴入饱和的FeCl3溶液,下列哪个变化的说法正确[ ]
A.水解平衡向正反应方向移动
B.水解平衡向逆反应方向移动
C.溶液中H+浓度增大
D.Fe3+的水解程度增大
查看习题详情和答案>>
B.水解平衡向逆反应方向移动
C.溶液中H+浓度增大
D.Fe3+的水解程度增大
下列对各种体系的叙述中,不正确的是( )
查看习题详情和答案>>
| A.在含FeCl2杂质的FeCl3溶液中通入足量C12后,充分加热除去过量Cl2,得到较纯净的FeCl3溶液 |
| B.一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) |
| C.常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动 |
| D.处理锅炉水垢中的CaSO4时,先用饱和Na2CO3溶液处理,再加入盐酸,水垢就会溶解 |
下列对各种体系的叙述中,不正确的是( )
A.在含FeCl2杂质的FeCl3溶液中通入足量C12后,充分加热除去过量Cl2,得到较纯净的FeCl3溶液
B.一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+)
C.常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动
D.处理锅炉水垢中的CaSO4时,先用饱和Na2CO3溶液处理,再加入盐酸,水垢就会溶解
查看习题详情和答案>>
A.在含FeCl2杂质的FeCl3溶液中通入足量C12后,充分加热除去过量Cl2,得到较纯净的FeCl3溶液
B.一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+)
C.常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动
D.处理锅炉水垢中的CaSO4时,先用饱和Na2CO3溶液处理,再加入盐酸,水垢就会溶解
查看习题详情和答案>>
高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。

⑴请完成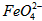 与水反应的化学方程式:
与水反应的化学方程式: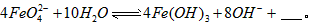
 在处理水的过程中所起的作用是____________和_____________。
在处理水的过程中所起的作用是____________和_____________。
⑵将适量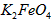 配制成c(
配制成c(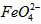 )=1.0mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(
)=1.0mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(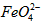 )的变化,结果见图I。第(1)题中的反应为
)的变化,结果见图I。第(1)题中的反应为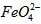 的变化的主反应,则温度对该反应的反应速率和平衡移动的影响是__________________;发生反应的△H_________0(填“﹥”、“﹤”或“=”)。
的变化的主反应,则温度对该反应的反应速率和平衡移动的影响是__________________;发生反应的△H_________0(填“﹥”、“﹤”或“=”)。
⑶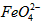 在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是________(填字母)。
在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是________(填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=2的这种溶液中加KOH溶液至pH=10,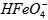 的分布分数先增大后减小
的分布分数先增大后减小
C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为: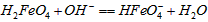
D.向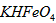 稀溶液加入水的过程中,pH可能增大也可能减小
稀溶液加入水的过程中,pH可能增大也可能减小
E.等体积等浓度的KOH溶液与溶液混合后溶液中的离子浓度大小关系为:
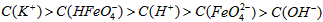
⑷Fe(OH)3在水中存在着沉淀溶解平衡:Fe(OH)3(s)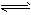 Fe3+(aq)+3OH-(aq),已知25℃时,溶度积常数
Fe3+(aq)+3OH-(aq),已知25℃时,溶度积常数
Ksp[Fe(OH)3]=4.0×10-38。某FeCl3溶液中c(Fe3+)=4.0×10-5 mol·L-1,在25℃时如果要生成Fe(OH)3沉淀,
需要向FeCl3溶液中加入碱溶液来调节溶液的pH,则必须使所得混合溶液的pH大于_________。
查看习题详情和答案>>
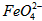 与水反应的化学方程式:
与水反应的化学方程式: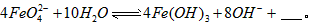
 在处理水的过程中所起的作用是____________和_____________。
在处理水的过程中所起的作用是____________和_____________。⑵将适量
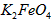 配制成c(
配制成c(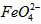 )=1.0mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(
)=1.0mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(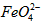 )的变化,结果见图I。第(1)题中的反应为
)的变化,结果见图I。第(1)题中的反应为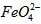 的变化的主反应,则温度对该反应的反应速率和平衡移动的影响是__________________;发生反应的△H_________0(填“﹥”、“﹤”或“=”)。
的变化的主反应,则温度对该反应的反应速率和平衡移动的影响是__________________;发生反应的△H_________0(填“﹥”、“﹤”或“=”)。⑶
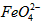 在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是________(填字母)。
在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是________(填字母)。 A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=2的这种溶液中加KOH溶液至pH=10,
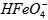 的分布分数先增大后减小
的分布分数先增大后减小C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:
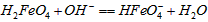
D.向
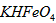 稀溶液加入水的过程中,pH可能增大也可能减小
稀溶液加入水的过程中,pH可能增大也可能减小E.等体积等浓度的KOH溶液与溶液混合后溶液中的离子浓度大小关系为:
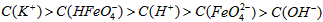
⑷Fe(OH)3在水中存在着沉淀溶解平衡:Fe(OH)3(s)
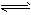 Fe3+(aq)+3OH-(aq),已知25℃时,溶度积常数
Fe3+(aq)+3OH-(aq),已知25℃时,溶度积常数Ksp[Fe(OH)3]=4.0×10-38。某FeCl3溶液中c(Fe3+)=4.0×10-5 mol·L-1,在25℃时如果要生成Fe(OH)3沉淀,
需要向FeCl3溶液中加入碱溶液来调节溶液的pH,则必须使所得混合溶液的pH大于_________。