网址:http://m.1010jiajiao.com/timu3_id_80951[举报]
下表是Na、Mg、Si、S、Br五种元素的单质的沸点,其中b、e均是热和电的良导体。
|
单质 |
a |
b |
c |
d |
e |
|
沸点(℃) |
58.8 |
882.9 |
444.7 |
2 355 |
1 107 |
(1) a的元素在元素周期表中的位置为________。
(2) 写出d的元素原子的电子式________;其最高价氧化物形成的晶体为________晶体(填类型),溶于强碱的离子方程式为________________________________________。
(3) c与氢形成的分子X的空间构型为________;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式___________________________________。
(4) 上述元素所能形成的简单离子中半径最小的是________(填离子符号),最高价氧化物对应水化物酸性最强的是________(填分子式),e元素与N元素形成化合物的电子式为____________________________。
(5) b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是________。
查看习题详情和答案>>
下表是Na、Mg、Si、S、Br五种元素的单质的沸点,其中b、e均是热和电的良导体。
| 单质 | a | b | c | d | e |
| 沸点(℃) | 58.8 | 882.9 | 444.7 | 2 355 | 1 107 |
(1) a的元素在元素周期表中的位置为________。
(2) 写出d的元素原子的电子式________;其最高价氧化物形成的晶体为________晶体(填类型),溶于强碱的离子方程式为________________________________________。
(3) c与氢形成的分子X的空间构型为________;写出X的水溶液与足量b元素的最高价氧化物对应水化物反应的离子方程式___________________________________。
(4) 上述元素所能形成的简单离子中半径最小的是________(填离子符号),最高价氧化物对应水化物酸性最强的是________(填分子式),e元素与N元素形成化合物的电子式为___________________________________。
(5) b元素与氯元素形成的化合物Y的晶体中,1个晶胞内含有的基本微粒及个数是________。
查看习题详情和答案>>下表是Na、Fe、Si、H、C、O六种元素的单质熔点数据,请问答下列问题:

(2)b与e、b与f均可形成AB2型化合物,则b与f形成AB2 型化合物中A采取的杂化方式为___。
(3)a与f可形成一种称为卡宾的物质。卡宾由1个f与2个a 构成。a与f形成两个σ键,f原子中最外层还有一对孤对电子,用价层电子对互斥理论推断,卡宾中两个共价键的夹角 ____(填“>”“<”或“=”)120°。
(4)元素d的化合物灼烧时呈现的焰火与___有关。
(5)b与f形成AB型化合物,其分子结构式为___ 该分子中π键数目为___。
(6)b与c形成原子个数比为4:3的化合物的晶胞同NaCl。则该离子化合物的一个晶胞中含b原子个数为___。
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | F | Na | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)Ne 原子结构示意图为
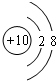
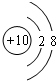
(3)C 与N 中,原子半径较小的是
(4)氯水具有漂白作用,是由于其中含有
(5)元素最高价氧化物对应的水化物中,碱性最强的是
(6)元素硅的氧化物常用于制造
(7)如图为某有机物的球棍模型(其中
 代表氢原子代表
代表氢原子代表  碳原子),
碳原子),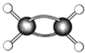 该有机物中碳元素与氢元素的质量比m(C):m(H)=
该有机物中碳元素与氢元素的质量比m(C):m(H)=
| ||
| ||
| 周期 主族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)Cl原子结构示意图为
(3)第三周期元素中,最高价氧化物对应水化物碱性最强的是
(4)O和N中,原子半径较大的是
(5)“高钙牛奶”中的钙是指
(6)Cl的气态氢化物的稳定性比F的气态氢化物
(7)常温下为红棕色气体的氧化物的化学式是
(8)镁是一种重要的金属材料,工业上采用电解熔融氯化镁获得金属镁,该反应的化学方程式为
(9)S元素形成的一种氢化物的化学式是