网址:http://m.1010jiajiao.com/timu3_id_78697[举报]
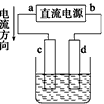
B.c为阴极、d为阳极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
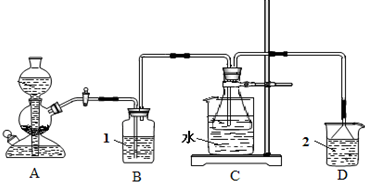
(1)碳酸氢钠受热分解的化学方程式为
| ||
| ||
(2)实验中,要注意控制二氧化碳的通入速度(以出现能数得清的连续气泡为好)和水浴的温度.实验中不能过快的通入二氧化碳的目的是
实验时,锥形瓶中产生了NH4HCO3、NaCl、NaHCO3和NH4Cl的混合液.右表是四种化合物在部分温度下的溶解度.由表中数据可知,反应时水浴的温度不能超过
| 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | 分解 |
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 |
(Ⅰ)如图1表示一个电解池,装有电解液a;通过导线与直流电源相连.请回答以下问题:

(1)若a是饱和NaCl溶液,X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为______.在X极附近观察到的实验现象是______.
②检验Y电极反应产物的方法是______.
(2)若a是CuSO4溶液,要用电解方法精炼粗铜,则Y电极的材料是______,X极发生______反应(填“氧化”或“还原”)
(Ⅱ)某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池如图2,得到的实验数据如下表所示:(已知果汁是显酸性的)
| 实验编号 | 水果种类 | 电极间距离/cm | 电流大小/?A |
| ① | 西红柿 | 1 | 98.7 |
| ② | 西红柿 | 2 | 72.5 |
| ③ | 苹 果 | 2 | 27.2 |
(2)能表明水果种类对电流大小有影响的实验编号是______和______.
(3)图2所示的装置中,正极附近区域的C(H+)将______(填“增大”、“减小”、“不变”).
(Ⅲ)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图3所示:
a、b两个电极均由多孔的碳块组成.写出该电池负极的电极反应式:______.
近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题.
(1)有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液.
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸.
(Ⅲ)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用.
①写出步骤(I)反应的化学方程式:________
②写出步骤(Ⅲ)反应的离子方程式:________
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42一而实现SO2的回收利用.某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42一的转化率.
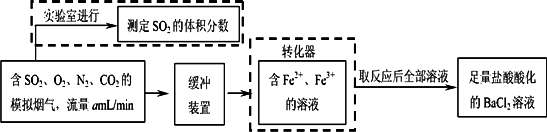
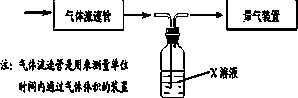
①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号)________.(参考:还原性SO2>I->Br->Cl-)
A.碘的淀粉溶液
B.酸性高锰酸钾溶液
C.氢氧化钠溶液
D.氯化钡溶液
②若上述实验是在标准状况下进行的,X是已知体积和物质的量浓度的溶液,欲测定转化器中SO2氧化成SO42一的转化率,已知气体流速,还需测定的数据是________和加入盐酸酸化的氯化钡溶液后生成沉淀的质量.
(3)
为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在消化细菌的作用下将NH4+氧化为NO3-:NH4++2O2=NO3-+2H++H2O,然后加入甲醇(CH3OH),NO3-和甲醇转化为
两种无毒气体.请写出加入甲醇后反应的离子方程式________.(13分)近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
⑴有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下: ( I )将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。(III)将盐酸加入NaHSO3溶液中得SO2气体回收,生成的NaCl循环利用。
① 写出步骤(I)反应的化学方程式:
② 写出步骤(III)反应的离子方程式:
⑵还有学者提出利用 Fe 2十、Fe3十等离子的催化作用,常温下将SO2氧化成SO42一而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42一的转化率。
① 该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号) 。(参考:还原性SO2 > I- >Br->Cl-)
A.碘的淀粉溶液 B.酸性高锰酸钾溶液
C.氢氧化钠溶液 D.氯化钡溶液
② 若上述实验是在标准状况下进行的,X是已知体积和物质的量浓度的溶液,欲测定转化器中SO2氧化成SO42一的转化率,已知气体流速,还需测定的数据是 和加入盐酸酸化的氯化钡溶液后生成沉淀的质量。
(3) 新型氨法烟气脱硫技术采用氨吸收烟气中SO2生成亚硫酸铵和亚硫酸氢铵,再用一定量的磷酸进行反应,在反应回收SO2后的混合物中通入适量的氨气得到一种产品。该技术的优点是 。
(4) 为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+Sx 、
CO+Sx=COS、2COS+SO2=2CO2+
Sx 。其中COS中“C”化合价为 。
(5)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在消化细菌的作用下将
NH4+氧化为NO3-:NH4++2O2=NO3-+2H++H2O,然后加入甲醇【CH3OH】,NO3-和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式 。
查看习题详情和答案>>