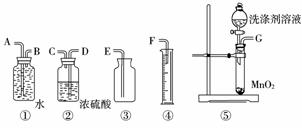
摘要:15.把NaOH.MgCl2.AlCl3三种固体组成的混合物溶于 足量水后有1.16 g白色沉淀.在所得的悬浊液中逐滴 加入1 mol·L-1 HCl溶液.加入HCl溶液的体积V与 生成沉淀的质量m的关系如图所示.试回答: (1)A点沉淀物的化学式为 ,B点沉淀物的化学式为 . (2)原混合物中的MgCl2的物质的量为 .AlCl3的物质的量为 .NaOH的物 质的量为 . (3)HCl溶液在C点的加入量是 . 解析:(1)盐酸加入量在0-10 mL时.沉淀的质量没有改变.说明未加盐酸时.沉淀物为 Mg(OH)2.溶液为NaAlO2和NaOH的混合液.其过程中加盐酸是中和剩余的NaOH.A 处的悬浊液为Mg(OH)2.NaAlO2.NaCl.则原混合物中n(MgCl2)=1.16 g/58 g·mol-1=0.02 mol. (2)加入盐酸10-30 mL过程时.发生反应为:AlO+H++H2O===Al(OH)3↓.B沉淀的化 学式为Mg(OH)2.Al(OH)3.原溶液中n(AlCl3)=×10-3 L×1 mol/L=0.02 mol.B 点沉淀量达到最大值.其中溶液为NaCl溶液.所以n=n(HCl)=30×10-3 L×1 mol/L=0.03 mol. 2.Al(OH)3完全溶解时.所消耗盐酸的体积为V′.V′×10-3 L/mL×1 mol/L =0.02 mol×2+0.02 mol×3.∴V′=100 mL.∴C点表示加入了130 mL的盐酸. 答案:2 Mg(OH)2.Al(OH)3 (2)0.02 mol 0.02 mol 0.03 mol (3)130 Ml
网址:http://m.1010jiajiao.com/timu3_id_78635[举报]
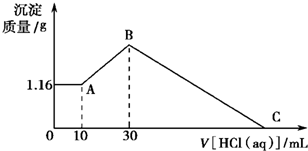 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:?
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示,试回答:?(1)A点→B点反应的离子方程式为
H2O+AlO2-+H+=Al(OH)3↓
H2O+AlO2-+H+=Al(OH)3↓
.(2)原混合物中AlCl3的物质的量为
0.02mol
0.02mol
,NaOH的物质的量为0.13 mol
0.13 mol
.(3)HCl溶液在C点的加入量是
130mL
130mL
.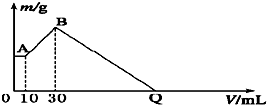 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得悬浊液中逐滴加入1mol?L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:(1)A点的沉淀物的化学式为
Mg(OH)2
Mg(OH)2
;AB段反应的离子方程式为H2O+AlO2-+H+=Al(OH)3↓
H2O+AlO2-+H+=Al(OH)3↓
?(2)Q点溶液中的阳离子有
Na+、Mg2+、Al3
Na+、Mg2+、Al3
(3)原混合物AlCl3的质量是
2.67
2.67
g,NaOH的质量是5.2
5.2
g?
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16 g 白色沉淀,在所得的悬浊液中逐滴加入1 mol·L-1 HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示。试完成下列问题:

(1)A点沉淀物的化学式为____________;B点沉淀物的化学式为___________。
(2)原混合物中的MgCl2的物质的量为___________,AlCl3的物质的量为___________,NaOH的物质的量为___________。
(3)HCl溶液在Q点的加入量是___________。
查看习题详情和答案>>
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量的水后,产生1.16 g白色沉淀,再向所得浊液中加入1.00 mol·L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的关系如下图所示。
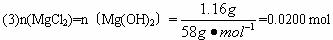
试完成下列问题:
(1)A点的沉淀物的化学式为____________,理由是______________________。
(2)写出A点到B点发生反应的离子方程式_____________________________。
(3)原混合物中MgCl2的质量是________g。AlCl3的质量是________g,NaOH的质量是________g。
(4)C点HCl溶液的体积为________mL。
查看习题详情和答案>>