摘要:10.向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液反应时.溶液褪色总是先慢后快.为了探究此反应速率由小变大的原因.设计如下实验 已知:①MnO在酸性环境下的还原产物是Mn2+, ②草酸是二元弱酸.有毒.温度较高时分解. (1)0.10mol/L H2C2O4溶液的配制:K^S*5U.C#O 实验室欲配制100mL 0.10mol/L H2C2O4 溶液.需要用托盘天平称取草酸晶体(H2C2O4·2H2O) g,实验中需要用到的玻璃仪器除了玻璃棒.胶头滴管外还有: . (2)反应速率变化的探究 取4支试管.按以下四种方案分别加入相应的试剂.使其发生反应.四支试管中均可观察到有气泡产生.且溶液的颜色变化均如下:紫红色→红色→橙红色→橙色→黄色→无色.但溶液褪为无色所需的时间不同.如下表所示:(表中“- 表示未加入该试剂) 实验 编号 温度 0.10mol/L 草酸溶液 稀硫酸 溶液 MnSO4固体 0.10 mol/L KMnO4溶液 褪色 时间 1 65℃ 5mL - - 1mL 100s 2 65℃ 5mL 10滴 - 1mL 90s 3 75℃ 5mL 10滴 - 1mL 40s 4 75℃ 5mL 10滴 加入少许 1mL 3s ①H2C2O4溶液与酸性的KMnO4溶液反应的离子方程式为 ; ②设计对比实验1.2的目的是: ; ③由表中数据可以得出.温度对该化学反应速率的影响是: ; 为了加快该反应的反应速率.是不是水浴的温度越高越好? ; ④由以上4个实验.还可以得出的一个结论是: ⑤若为了探究浓度对该反应速率的影响.则在所设计的实验中最好是增大 (填“草酸 或“高锰酸钾 )溶液的浓度.以减少实验误差.
网址:http://m.1010jiajiao.com/timu3_id_77869[举报]
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大.小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证.
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因;
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等.
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容.
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+) .
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是 .
(3)猜想Ⅱ可能是 .要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是 .
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
查看习题详情和答案>>
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因;
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等.
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容.
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+)
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是
(3)猜想Ⅱ可能是
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
| 试管A | 试管B | |
| 加入试剂 | ||
| (预期)实验现象 (褪色时间) |
||
| 结论 | 猜想Ⅱ正确 | |
I.下列实验操作、试剂保存方法和实验室事故处理,一定正确的是______(填序号).
A.不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
B.制备氢氧化铁胶体时,应向沸水中逐滴滴加1~2mL饱和的FeC13溶液,并继续加 热到液体呈透明的红褐色为止
C.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液滴在用蒸馏水湿润过的pH试纸上,并与标准比色卡比较
D.实验室中,浓硝酸保存在带橡胶塞的棕色细口试剂瓶中
E.除去蛋白质溶液中混有的NaC1,可以先加入AgNO3溶液,然后过滤
F.在进行反应热测定时,为保证实验的准确性,我们可以采取以下具体措施:使用碎泡沫以起到隔热保温的作用、使用铜质搅拌棒进行搅拌、使用的酸碱正好反应、进行两到三次实验,取平均值
II.石灰石的主要成份是碳酸钙,含氧化钙约40~50%,较好的石灰石含CaO约45~53%.此外还有SiO2、Fe2O3、Al2O3及MgO等杂质.测定石灰石中钙的含量时将样品溶于盐酸,加入草酸铵溶液,在中性或碱性介质中生成难溶的草酸钙沉淀 (CaC2O4?H2O),将所得沉淀过滤、洗净,用硫酸溶解,用标准高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,间接求出钙的含量.涉及的化学反应为:H2C2O4+MnO4-+H+→Mn2++CO2↑+H2O(未配平).CaC2O4 沉淀颗粒细小,易沾污,难于过滤.为了得到纯净而粗大的结晶,通常在含Ca2+的酸性溶液中加入饱和 (NH4)2C2O4,由于C2O42-浓度很低,而不能生成沉淀,此时向溶液中滴加氨水,溶液中C2O42-浓度慢慢增大,可以获得颗粒比较粗大的CaC2O4沉淀.沉淀完毕后,pH应在3.5~4.5,这样可避免其他难溶钙盐析出,又不使CaC2O4溶解度太大.根据以上材料回答下列问题:
(1)样品溶于盐酸后得到的沉淀物主要是______
(2)沉淀 CaC2O4要加入沉淀剂饱和的 (NH4)2C2O4 溶液,为什么?______
(3)工业中通常先用0.1%草酸铵溶液洗涤沉淀,再用冷的蒸馏水洗涤,其目的是:______
(4)若开始用去m g样品,最后滴定用去浓度为c mol/L 的KMnO4 溶液V mL,推出CaO含量与 KMnO4的定量计算关系.ω%=______.
查看习题详情和答案>>
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 有毒,具有腐蚀性,易溶于水,二元弱酸. 100℃开始升华,157℃时开始分解. 草酸与浓硫酸混合加热产生CO2、CO和H2O. 草酸钙和草酸氢钙均为白色不溶物 |

(1)用字母表示接口的正确连接顺序.
a→b→c→______→______→d→e→______→______→______→______→尾气处理
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,原因是______;请你提出改进意见______.
(3)利用改进后装置进行的实验时,要先加热______ 装置,(填“A”、“B”、“C”、“D”、“E”,下同)后加热______ 装置;能证明分解产物中有CO的实验依据是______.
[实验二]探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有______.
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下的对比实验:
| 实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(S) (g) | 褪色时间 (S) | ||
| C(mol?L-1) | V(mL) | C(mol?L-1) | V(mL) | |||
| 实验1 | 0.1 | 2 | 0.01 | 4 | 0 | 30 |
| 实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
[实验一]根据下图提供的仪器和试剂(可重复使用),设计实验证明草酸的受热分解产物中含有CO2和CO(部分夹持仪器和加热装置省略)
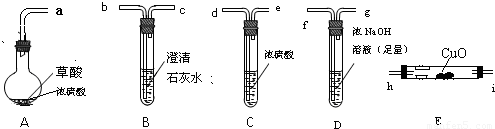
(1)用字母表示接口的正确连接顺序.
a→b→c→______→______→d→e→______→______→______→______→尾气处理
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,原因是______;请你提出改进意见______.
(3)利用改进后装置进行的实验时,要先加热______ 装置,(填“A”、“B”、“C”、“D”、“E”,下同)后加热______ 装置;能证明分解产物中有CO的实验依据是______.
[实验二]探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有______.
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下的对比实验:
该对比实验的结论是______.
查看习题详情和答案>>
| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 有毒,具有腐蚀性,易溶于水,二元弱酸. 100℃开始升华,157℃时开始分解. 草酸与浓硫酸混合加热产生CO2、CO和H2O. 草酸钙和草酸氢钙均为白色不溶物 |

(1)用字母表示接口的正确连接顺序.
a→b→c→______→______→d→e→______→______→______→______→尾气处理
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,原因是______;请你提出改进意见______.
(3)利用改进后装置进行的实验时,要先加热______ 装置,(填“A”、“B”、“C”、“D”、“E”,下同)后加热______ 装置;能证明分解产物中有CO的实验依据是______.
[实验二]探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有______.
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下的对比实验:
| 实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(S) (g) | 褪色时间 (S) | ||
| C | V(mL) | C | V(mL) | |||
| 实验1 | 0.1 | 2 | 0.01 | 4 | 30 | |
| 实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
查看习题详情和答案>>
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
[实验一]根据下图提供的仪器和试剂(可重复使用),设计实验证明草酸的受热分解产物中含有CO2和CO(部分夹持仪器和加热装置省略)

(1)用字母表示接口的正确连接顺序.
a→b→c→
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,原因是
(3)利用改进后装置进行的实验时,要先加热
[实验二]探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下的对比实验:
该对比实验的结论是
查看习题详情和答案>>
| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 有毒,具有腐蚀性,易溶于水,二元弱酸. 100℃开始升华,157℃时开始分解. 草酸与浓硫酸混合加热产生CO2、CO和H2O. 草酸钙和草酸氢钙均为白色不溶物 |

(1)用字母表示接口的正确连接顺序.
a→b→c→
f
f
→g
g
→d→e→h
h
→i
i
→b
b
→c
c
→尾气处理(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,原因是
草酸蒸气也可以使澄清石灰水变浑浊,无法确定二氧化碳的存在,
草酸蒸气也可以使澄清石灰水变浑浊,无法确定二氧化碳的存在,
;请你提出改进意见在A前添加一个盛水的洗气瓶,除去草酸蒸气
在A前添加一个盛水的洗气瓶,除去草酸蒸气
.(3)利用改进后装置进行的实验时,要先加热
A
A
装置,(填“A”、“B”、“C”、“D”、“E”,下同)后加热E
E
装置;能证明分解产物中有CO的实验依据是E中黑色氧化铜变红,E后的澄清石灰水变浑浊
E中黑色氧化铜变红,E后的澄清石灰水变浑浊
.[实验二]探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有
还原性
还原性
.(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下的对比实验:
| 实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(S) (g) |
褪色时间 (S) | ||
| C(mol?L-1) | V(mL) | C(mol?L-1) | V(mL) | |||
| 实验1 | 0.1 | 2 | 0.01 | 4 | 0 | 30 |
| 实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
反应生成的Mn2+有催化作用,加快了反应速率
反应生成的Mn2+有催化作用,加快了反应速率
.