题目内容
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 有毒,具有腐蚀性,易溶于水,二元弱酸. 100℃开始升华,157℃时开始分解. 草酸与浓硫酸混合加热产生CO2、CO和H2O. 草酸钙和草酸氢钙均为白色不溶物 |
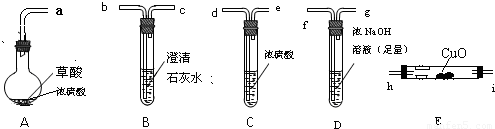
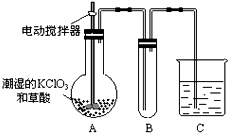
(1)用字母表示接口的正确连接顺序.
a→b→c→______→______→d→e→______→______→______→______→尾气处理
(2)用上图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,原因是______;请你提出改进意见______.
(3)利用改进后装置进行的实验时,要先加热______ 装置,(填“A”、“B”、“C”、“D”、“E”,下同)后加热______ 装置;能证明分解产物中有CO的实验依据是______.
[实验二]探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,可推测草酸可能具有______.
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下的对比实验:
| 实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(S) (g) | 褪色时间 (S) | ||
| C | V(mL) | C | V(mL) | |||
| 实验1 | 0.1 | 2 | 0.01 | 4 | 30 | |
| 实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
【答案】分析:(1)二氧化碳能使澄清的石灰水变浑浊,一氧化碳检验还原性,能还原黑色的氧化铜,生成的二氧化碳用澄清的石灰水检验,据此根据二氧化碳和一氧化碳的性质进行排序;
(2)根据表格知,草酸具有酸性,能和碱性物质反应,且草酸钙不溶于水,为防止草酸蒸气的干扰,在将气体通入澄清石灰水之前,应先除去草酸蒸气;
(3)一氧化碳和氧气反应在一定范围内易产生爆炸,为防止产生安全事故发生,应先制取气体,用生成的气体除去装置中的氧气;一氧化碳具有还原性,能还原黑色的氧化铜生成铜单质,且生成二氧化碳;
(4)根据酸性高锰酸钾的性质确定草酸的性质;
(5)将两个实验进行对比,从而得出结论.
解答:解:(1)为证明草酸的受热分解产物中含有CO2和CO,先将混合气体通入澄清的石灰水检验二氧化碳,如果澄清的石灰水变浑浊,则证明含有二氧化碳气体,再用氢氧化钠溶液吸收二氧化碳,再将洗气后的气体进行干燥,然后将气体再通过黑色的氧化铜装置,一氧化碳和黑色的氧化铜反应生成铜和二氧化碳,再用澄清的石灰水检验二氧化碳是否存在,如果澄清石灰水变浑浊,则证明该混合气体中含有一氧化碳,注意洗气装置、干燥装置中的导气管应该是“长进,短出”
所以其排序是:a→b→c→( f)→( g)→d→e→(h )→(i )→(b )→(c ),
故答案为:a→b→c→( f)→( g)→d→e→(h )→(i )→(b )→(c );
(2)根据表格知,草酸100℃开始升华,且草酸具有酸性,和氢氧化钙反应生成的草酸钙不溶于水,二氧化碳和氢氧化钙反应也生成碳酸钙沉淀,所以制取的气体中含有草酸蒸气而干扰二氧化碳的检验,要检验二氧化碳首先要除去草酸蒸气,所以在A前添加一个盛水的洗气瓶,除去草酸,
故答案为:草酸蒸气也可以使澄“清石灰水变浑浊,无法确定二氧化碳的存在,故应在A前添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管);
(3)一氧化碳和氧气反应在一定范围内易产生爆炸,为防止产生安全事故发生,应先制取气体,用生成的气体除去装置中的氧气,所以应先加热A后加热E;一氧化碳具有还原性,能还原黑色的氧化铜生成铜单质,且生成二氧化碳,二氧化碳能澄清石灰水变浑浊,所以反应现象是:E中黑色氧化铜变红,E后的澄清石灰水变浑浊;
故答案为:A,E;E中黑色氧化铜变红,E后的澄清石灰水变浑浊;
(4)酸性高锰酸钾具有强氧化性,草酸能使酸性高锰酸钾溶液褪色,说明草酸具有还原性,故答案为:还原性;
(5)通过两组实验比较知,其它条件相同,加入硫酸锰的反应时间短,说明该实验反应速率快,所以证明反应生成的Mn2+有催化作用,加快了反应速率,故答案为:反应生成的Mn2+有催化作用,加快了反应速率.
点评:本题考查了实验设计,难度较大,注意检验二氧化碳和一氧化碳的混合物中,要先检验二氧化碳再检验一氧化碳,为易错点.
(2)根据表格知,草酸具有酸性,能和碱性物质反应,且草酸钙不溶于水,为防止草酸蒸气的干扰,在将气体通入澄清石灰水之前,应先除去草酸蒸气;
(3)一氧化碳和氧气反应在一定范围内易产生爆炸,为防止产生安全事故发生,应先制取气体,用生成的气体除去装置中的氧气;一氧化碳具有还原性,能还原黑色的氧化铜生成铜单质,且生成二氧化碳;
(4)根据酸性高锰酸钾的性质确定草酸的性质;
(5)将两个实验进行对比,从而得出结论.
解答:解:(1)为证明草酸的受热分解产物中含有CO2和CO,先将混合气体通入澄清的石灰水检验二氧化碳,如果澄清的石灰水变浑浊,则证明含有二氧化碳气体,再用氢氧化钠溶液吸收二氧化碳,再将洗气后的气体进行干燥,然后将气体再通过黑色的氧化铜装置,一氧化碳和黑色的氧化铜反应生成铜和二氧化碳,再用澄清的石灰水检验二氧化碳是否存在,如果澄清石灰水变浑浊,则证明该混合气体中含有一氧化碳,注意洗气装置、干燥装置中的导气管应该是“长进,短出”
所以其排序是:a→b→c→( f)→( g)→d→e→(h )→(i )→(b )→(c ),
故答案为:a→b→c→( f)→( g)→d→e→(h )→(i )→(b )→(c );
(2)根据表格知,草酸100℃开始升华,且草酸具有酸性,和氢氧化钙反应生成的草酸钙不溶于水,二氧化碳和氢氧化钙反应也生成碳酸钙沉淀,所以制取的气体中含有草酸蒸气而干扰二氧化碳的检验,要检验二氧化碳首先要除去草酸蒸气,所以在A前添加一个盛水的洗气瓶,除去草酸,
故答案为:草酸蒸气也可以使澄“清石灰水变浑浊,无法确定二氧化碳的存在,故应在A前添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管);
(3)一氧化碳和氧气反应在一定范围内易产生爆炸,为防止产生安全事故发生,应先制取气体,用生成的气体除去装置中的氧气,所以应先加热A后加热E;一氧化碳具有还原性,能还原黑色的氧化铜生成铜单质,且生成二氧化碳,二氧化碳能澄清石灰水变浑浊,所以反应现象是:E中黑色氧化铜变红,E后的澄清石灰水变浑浊;
故答案为:A,E;E中黑色氧化铜变红,E后的澄清石灰水变浑浊;
(4)酸性高锰酸钾具有强氧化性,草酸能使酸性高锰酸钾溶液褪色,说明草酸具有还原性,故答案为:还原性;
(5)通过两组实验比较知,其它条件相同,加入硫酸锰的反应时间短,说明该实验反应速率快,所以证明反应生成的Mn2+有催化作用,加快了反应速率,故答案为:反应生成的Mn2+有催化作用,加快了反应速率.
点评:本题考查了实验设计,难度较大,注意检验二氧化碳和一氧化碳的混合物中,要先检验二氧化碳再检验一氧化碳,为易错点.

练习册系列答案
相关题目
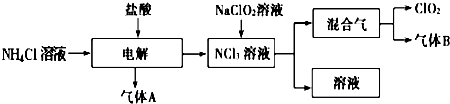
 用二氧化氯(ClO2)、高铁酸钠(Na2FeO4摩尔质量为166g?mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯(ClO2)、高铁酸钠(Na2FeO4摩尔质量为166g?mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.