摘要:24.已知抛物线与轴的交点是A.且经过点C(2.8) . (1)求该抛物线的解析式, (2)求该抛物线的顶点坐标.
网址:http://m.1010jiajiao.com/timu3_id_7758[举报]
某化学兴趣小组设计出下列粗盐提纯的实验方案,请你一起来完成以下问题.
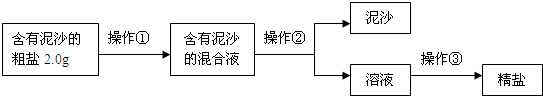
(1)操作①②③的名称依次是
A 5mL B 8mL C 12mL
(2)操作②所需的玻璃仪器有
(3)实施操作③时玻璃棒要不断
(4)兴趣小组的同学通过正确的计算发现,实验所得精盐的产率比该粗盐中氯化钠的实际含量偏低,则可能的原因是
A.过滤时滤纸有破损 B.蒸发时有固体溅出
C.溶解含有泥沙的粗盐时,加入的水量不足
D.将含有泥沙的混合液全部倾倒入过滤器后,用清水洗涤玻璃棒和烧杯并将该液体一并倒入过滤器
E.转移精盐时,玻璃棒、蒸发皿中有残留的固体
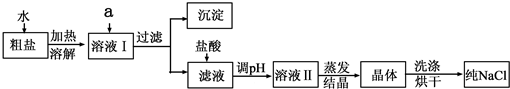
(5)兴趣小组成员查阅资料后得知,粗盐中除含NaCl、泥沙外,还含有少量MgCl2、CaCl2、Na2SO4等杂质.而过滤是一种将
提供的试剂有:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液.
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、过量的
②在滤液中加盐酸的作用是
(6)该兴趣小组现利用提纯后的精盐配制200g溶质质量分数为0.9%的生理盐水,需要精盐的质量为
查看习题详情和答案>>

(1)操作①②③的名称依次是
沉降
沉降
、过滤
过滤
、蒸发
蒸发
,在实施操作①前需先将粗盐磨碎,其作用是便于溶解并除去其中的杂质
便于溶解并除去其中的杂质
,同时该操作①所需水的最佳量是B
B
(已知20℃时食盐的溶解度是36g,填字母序号).A 5mL B 8mL C 12mL
(2)操作②所需的玻璃仪器有
烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
,若该操作结束后发现溶液仍浑浊,则可能原因是滤纸破损
滤纸破损
(任答一点原因,即可);(3)实施操作③时玻璃棒要不断
搅拌
搅拌
(填操作方法),直到大部分固体结晶析出
大部分固体结晶析出
时停止加热.(4)兴趣小组的同学通过正确的计算发现,实验所得精盐的产率比该粗盐中氯化钠的实际含量偏低,则可能的原因是
BCE
BCE
(填字母序号)A.过滤时滤纸有破损 B.蒸发时有固体溅出
C.溶解含有泥沙的粗盐时,加入的水量不足
D.将含有泥沙的混合液全部倾倒入过滤器后,用清水洗涤玻璃棒和烧杯并将该液体一并倒入过滤器
E.转移精盐时,玻璃棒、蒸发皿中有残留的固体

(5)兴趣小组成员查阅资料后得知,粗盐中除含NaCl、泥沙外,还含有少量MgCl2、CaCl2、Na2SO4等杂质.而过滤是一种将
泥沙
泥沙
与水分离的方法,因此上一套实验方案不能除去粗盐中的MgCl2、CaCl2、Na2SO4等杂质,为此,他们又重新设计了第二套实验方案.提供的试剂有:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液.
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、过量的
BaCl2溶液
BaCl2溶液
、过量的Na2CO3溶液
Na2CO3溶液
;②在滤液中加盐酸的作用是
除去过量的碳酸钠和氢氧化钠
除去过量的碳酸钠和氢氧化钠
;(6)该兴趣小组现利用提纯后的精盐配制200g溶质质量分数为0.9%的生理盐水,需要精盐的质量为
1.8
1.8
g,配制该溶液时所需要的水应选择500mL
500mL
(选填“50mL”、“100mL”或“500mL”)量筒,读数时,若视线仰视(其他操作无误),则所配制的溶液的溶质质量分数小于
小于
(选填“大于”、“小于”或“等于”)0.9%.9、现有甲、乙、丙、丁四种物质的无色溶液,已知乙与丙的溶液混合生成的沉淀不溶于甲的溶液,乙与丁的溶液混合生成的沉淀可溶于甲的溶液.则下列各组物质中符合此现象的是( )
|
查看习题详情和答案>>
(2013?门头沟区二模)化学兴趣小组的同学在实验室发现一瓶保HCl管不当,盛有无色溶液的试剂瓶,且标签破损,其残缺的标签中只剩下“Na”和“10%”字样.已知该溶液中的溶质是一种初中化学常见的化合物.
[相关资料]
Ⅰ.初中化学常见的含钠化合物有氯化钠、氢氧化钠、碳酸钠、碳酸氢钠.
Ⅱ.碱性的Na2CO3溶液与中性的CaCl2溶液能发生复分解反应.
Ⅲ.测定室温(20℃)时,四种物质的溶解度数据如下:
[验证溶液的成分]
(1)根据资料判断:该溶液不是
(2)进一步实验验证:请完成对实验过程的填写
由此,同学们得出结论:该溶液是碳酸钠溶液.老师指出该结论不严密.理由是:
查看习题详情和答案>>
[相关资料]
Ⅰ.初中化学常见的含钠化合物有氯化钠、氢氧化钠、碳酸钠、碳酸氢钠.
Ⅱ.碱性的Na2CO3溶液与中性的CaCl2溶液能发生复分解反应.
Ⅲ.测定室温(20℃)时,四种物质的溶解度数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解的质量/g | 36 | 109 | 21.5 | 9.6 |
(1)根据资料判断:该溶液不是
NaHCO3
NaHCO3
溶液.(2)进一步实验验证:请完成对实验过程的填写
| 实验 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| Ⅰ | 取样于试管中,向其中滴加无色酚酞溶液 | 无色溶液变红色 | 该溶液不可能是 NaCl NaCl 溶液,理由是NaCl溶液呈中性,不能使酚酞试液变色 NaCl溶液呈中性,不能使酚酞试液变色 |
| Ⅱ | 另取样于另一支试管中,向其中滴加足量的 稀盐酸(或稀硫酸) 稀盐酸(或稀硫酸) |
产生大量的气泡 | 该溶液为碳酸钠,有关反应的化学方程式为 Na2CO3+2HCl══2NaCl+H2O+CO2↑ Na2CO3+2HCl══2NaCl+H2O+CO2↑ |
氢氧化钠溶液在空气中敞开放置,发生变质,能产生与实验Ⅰ和Ⅱ相同现象
氢氧化钠溶液在空气中敞开放置,发生变质,能产生与实验Ⅰ和Ⅱ相同现象
.老师提示,不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl2
CaCl2
溶液,若观察到产生白色沉淀,且溶液红色不褪去
产生白色沉淀,且溶液红色不褪去
现象,即可说明该溶液中有氢氧化钠.某化学小组成功完成了如图所示实验(装置气密性良好),验证了二氧化碳的组成.
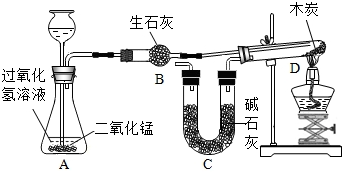
探究过程如下:
Ⅰ.称量装有干燥块状木炭的试管D,质量为50.7g,装有碱石灰的装置C质量为l12.3g,连接A、B、D装置;
Ⅱ.从长颈漏斗加入足量3%的过氧化氢溶液,连接C装置,点燃酒精灯;
Ⅲ.待D中发生反应,熄灭酒精灯,冷却;
Ⅳ.称量试管D及剩余固体的质量为50.1g,装置C的质量为114.5g
已知:碱石灰的成分是氧化钙和氢氧化钠(友情提示:氢氧化钠能与二氧化碳发生化学反应),木炭中的杂质不参与反应,B、C中所装药品足量,能完全吸收相关物质.请回答下列问题:
(1)装置A反应的化学方程式为 ,该反应属于 反应.
(2)装置B的作用是 .装置D中铁夹夹住试管的中上部的原因是 .酒精灯加热的作用是 .
(3)为减小误差,步骤Ⅲ冷却过程中需要注意的问题是 .
(4)根据实验数据计算参加反应的氧气的质量为(列式并计算) ,从而计算出二氧化碳中碳、氧元素的质量比.
查看习题详情和答案>>

探究过程如下:
Ⅰ.称量装有干燥块状木炭的试管D,质量为50.7g,装有碱石灰的装置C质量为l12.3g,连接A、B、D装置;
Ⅱ.从长颈漏斗加入足量3%的过氧化氢溶液,连接C装置,点燃酒精灯;
Ⅲ.待D中发生反应,熄灭酒精灯,冷却;
Ⅳ.称量试管D及剩余固体的质量为50.1g,装置C的质量为114.5g
已知:碱石灰的成分是氧化钙和氢氧化钠(友情提示:氢氧化钠能与二氧化碳发生化学反应),木炭中的杂质不参与反应,B、C中所装药品足量,能完全吸收相关物质.请回答下列问题:
(1)装置A反应的化学方程式为
(2)装置B的作用是
(3)为减小误差,步骤Ⅲ冷却过程中需要注意的问题是
(4)根据实验数据计算参加反应的氧气的质量为(列式并计算)
请结合如图所示实验装置回答有关问题:

(1)写出装置中标号仪器的名称.a
(2)写出一个实验室制取氧气的文字表达式
(3)用D装置收集氧气,检验氧气是否集满的方法是
(4)已知实验室制取二氧化碳的方法是用大理石和稀盐酸溶液在常温下反应制得,二氧化碳可溶于水,密度比空气大.则制取二氧化碳时可选用
查看习题详情和答案>>

(1)写出装置中标号仪器的名称.a
酒精灯
酒精灯
;b试管
试管
.(2)写出一个实验室制取氧气的文字表达式
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
,根据该反应原理,可选上图中| 加热 |
A
A
(填标号,下同)与C
C
组装一套制取氧气的装置.(3)用D装置收集氧气,检验氧气是否集满的方法是
将带火星的木条放在集气瓶口,若木条复燃,则证明已收集满.
将带火星的木条放在集气瓶口,若木条复燃,则证明已收集满.
(4)已知实验室制取二氧化碳的方法是用大理石和稀盐酸溶液在常温下反应制得,二氧化碳可溶于水,密度比空气大.则制取二氧化碳时可选用
B
B
发生装置(填A或B),收集二氧化碳可用D
D
装置.