摘要: 25 ℃.101 kPa下.碳.H2.CH4.葡萄糖的燃烧热依次为393.5 kJ/mol.285.8 kJ/mol.890.3 kJ/mol.2 800 kJ/mol.则下列热化学方程式正确的是( ) A.CΔH=-393.5 kJ/mol B.2H2ΔH=+571.6 kJ/mol C.CH4+2H2O(g) ΔH=-890.3 kJ/mol D.=3CO2 ΔH=-1 400 kJ/mol
网址:http://m.1010jiajiao.com/timu3_id_77341[举报]
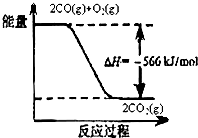 已知:
已知:(1)如图
(2)25℃、101kPa下:
①2Na (s)+
| 1 |
| 2 |
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol
根据以上信息判断,下列说法正确的是( )
查看习题详情和答案>>
