网址:http://m.1010jiajiao.com/timu3_id_74508[举报]
| A、将0.1mol CuSO4?5H2O晶体加入到100 mL水中,该溶液物质的量浓度为1 mol?L-1 | ||
| B、一定体积的浓硫酸(其中含0.2mol H2SO4)与足量的铜共热反应,生成SO2气体0.1mol | ||
| C、将34.2 g Al2(SO4)3溶于水配成100 mL溶液[Al2(SO4)3的相对质量为342J,取出10 mL该溶液中Al3+浓度为1 mol?L-1 | ||
D、KCl溶液的密度为1.174 g?cm-3,物质的量浓度为4.0 mol?L-1,则此溶液中KCl的质量分数为
|
下列说法中正确的是( )
| A.将0.1mol CuSO4·5H2O晶体加入到100 mL水中,该溶液物质的量浓度为1 mol?L?1 |
| B.一定体积的浓硫酸(其中含0.2mol H2SO4)与足量的铜共热反应,生成SO2气体0.1mol |
| C.将34.2 g Al2(SO4)3溶于水配成100 mL溶液[Al2(SO4)3的相对质量为342],取出10 mL该溶液中Al3+浓度为1 mol?L?1 |
D.KCl溶液的密度为1.174 g·cm?3,物质的量浓度为4.0 mol?L?1,则此溶液中KCl的质量分数为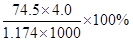 |
下列说法中正确的是( )
A.将0.1mol CuSO4·5H2O晶体加入到100 mL水中,该溶液物质的量浓度为1 mol?L?1
B.一定体积的浓硫酸(其中含0.2mol H2SO4)与足量的铜共热反应,生成SO2气体0.1mol
C.将34.2 g Al2(SO4)3溶于水配成100 mL溶液[Al2(SO4)3的相对质量为342],取出10 mL该溶液中Al3+浓度为1 mol?L?1
D.KCl溶液的密度为1.174 g·cm?3,物质的量浓度为4.0 mol?L?1,则此溶液中KCl的质量分数为
查看习题详情和答案>>
|
将34.2 g C12H22O11(蔗糖)溶解在100 mL水中.关于所组成的溶液,下列叙述中正确的是 | |
A. |
该溶液中溶质的物质的量浓度为1 mol·L-1 |
B. |
该溶液溶质的质量分数为 |
C. |
该溶液中溶质的物质的量浓度的确定还需知道溶液的密度 |
D. |
该溶液溶质的质量分数的确定还需知道溶液的密度 |
Ⅰ.有A、B、C三种无色溶液,它们分别是葡萄糖溶液、蔗糖溶液、淀粉溶液中的一种,甲同学做实验得出:
①B能发生银镜反应;
②A遇碘水变蓝色;
③A、C均能发生水解反应,水解液均能发生银镜反应.
试判断它们各是什么物质,并写出有关化学反应方程式:
(1)A是________,B是________,C是________.
(2)有关化学反应方程式:
①蔗糖水解:________.
②淀粉水解:________.
Ⅱ.乙同学将34.2 g蔗糖与16.2 g淀粉的混合物放入水中,在一定条件下使其完全水解,请回答:
(1)“一定条件”指的是________;
(2)判断淀粉和蔗糖已经水解的方法是________;
(3)完全水解后的溶液中有机物溶质的物质的量之比n(葡萄糖)∶n(果糖)=________.