摘要:氧气实验室制取的步骤:
网址:http://m.1010jiajiao.com/timu3_id_7315[举报]
实验室制取气体所需装置如下图所示.
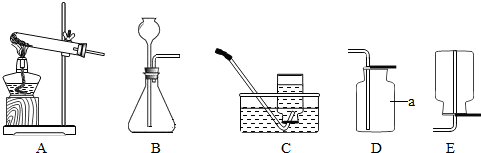
请回答以下问题:
(1)装置中标“a”的仪器名称是 .
(2)用高锰酸钾制取氧气时,所选用的发生装置是 (填字母序号,下同),其反应的化学方程式为 .制取时有以下主要操作步骤:①加热 ②把药品装入试管后固定在铁架台上 ③检查装置的气密性 ④熄灭酒精灯 ⑤用排水法收集气体⑥从水槽中移出导管.正确的操作顺序是 .
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置和收集装置是 ,其反应的化学方程式为 .
查看习题详情和答案>>

请回答以下问题:
(1)装置中标“a”的仪器名称是
(2)用高锰酸钾制取氧气时,所选用的发生装置是
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置和收集装置是
实验室制取氧气是初中化学阶段的重要实验.小元同学准确称取7.9g纯净的高锰酸钾加热一段时间后,收集到氧气580mL(标准状况).
(1)请写出两个实验室用固体反应物制取氧气的化学方程式: 、 .
(2)意外发现:
根据化学方程式计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾溶液呈墨绿色.
(3)提出假设:
小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气
假设2:锰酸钾也可以受热分解产生氧气
假设3:二氧化锰和锰酸钾受热都可以放出氧气
假设4: (只填一种)
(4)设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.
步骤1: →步骤2: →步骤三 →步骤4:干燥→步骤5:验证假设2
请简要叙述步骤5的操作 .
(5)得出结论:若观察到 ,则假设2成立;若观察到 ,则假设2不成立.
查看习题详情和答案>>
(1)请写出两个实验室用固体反应物制取氧气的化学方程式:
(2)意外发现:
根据化学方程式计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾溶液呈墨绿色.
(3)提出假设:
小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气
假设2:锰酸钾也可以受热分解产生氧气
假设3:二氧化锰和锰酸钾受热都可以放出氧气
假设4:
(4)设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.
步骤1:
请简要叙述步骤5的操作
(5)得出结论:若观察到
实验室制取氧气:
(1)药品: 或 或 .
(2)反应原理:
① .
②
③
(3)操作步骤:
下面是实验室加热高锰酸钾制取氧气并用排水法收集的主要操作步骤:
①点燃酒精灯,先使试管受热均匀,然后对准试管中的药品部位加热;
②将药品装入试管,用带导管的单孔橡皮塞塞紧试管;
③收集完毕,将导管从水槽中取出;
④检查装置的气密性;
⑤用排水法收集氧气;
⑥将试管固定在铁架台上;
⑦熄灭酒精灯.
正确的操作顺序是 .
(4)收集方法:
①由于氧气 ,可以用 收集;
②由于氧气 ,可以用 收集.
(5)检验方法: .
(6)验满方法: .
查看习题详情和答案>>
(1)药品:
(2)反应原理:
①
②
③
(3)操作步骤:
下面是实验室加热高锰酸钾制取氧气并用排水法收集的主要操作步骤:
①点燃酒精灯,先使试管受热均匀,然后对准试管中的药品部位加热;
②将药品装入试管,用带导管的单孔橡皮塞塞紧试管;
③收集完毕,将导管从水槽中取出;
④检查装置的气密性;
⑤用排水法收集氧气;
⑥将试管固定在铁架台上;
⑦熄灭酒精灯.
正确的操作顺序是
(4)收集方法:
①由于氧气
②由于氧气
(5)检验方法:
(6)验满方法:
实验室制取氧气大致可分为下列步骤:A、点燃酒精灯加热试管;B、检查装置的气密性;C、将高锰酸钾装入试管,用导管的塞子塞紧试管,并把它固定在铁架台上;D、用排水法收集氧气E、熄灭酒精灯F、将导管水槽中取出
(1)请按正确操作顺序排列序号 ;
(2)C操作中,高锰酸钾装入试管后应在管口 ,为了 (填原因)塞上塞子,据 确定试管夹夹持高度,并使管口稍向下倾斜,为了 (填原因);
(3)D操作中怎样才能使收集到的氧气基本上不含氮气? ;
(4)写出反应的符号表达式: .
查看习题详情和答案>>
(1)请按正确操作顺序排列序号
(2)C操作中,高锰酸钾装入试管后应在管口
(3)D操作中怎样才能使收集到的氧气基本上不含氮气?
(4)写出反应的符号表达式:
实验室制取氢气:
(1)实验原理:通过活泼金属与稀硫酸反应制取氢气通常是用金属
(2)反应方程式:
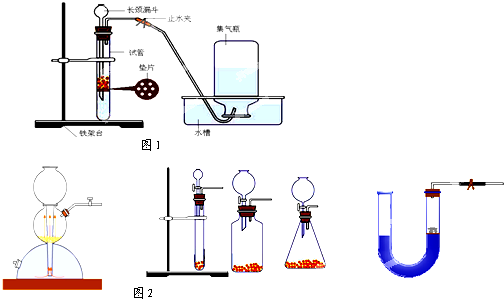
(3)反应装置如图1( 注意点):
A.长颈漏斗的下端需伸入垫片以下,形成液封,以及有利于固液可以分离.
B.由于氢气难溶于水,密度比空气小,故能用
C.优点:可以控制反应的
D.相似的氢气发生装置图2(固液制气,不需加热)
(4)实验步骤
A.按照实验要求,安装好实验仪器;
B.检查仪器装置的气密性:关闭止水夹,向分液漏斗中加入足量的水,若漏斗中的液面能存在一段水柱,并不持续下降,则说明
C.装药品:先将锌粒放在垫片上,打开止水夹后,向长颈漏斗中注入稀盐酸,发生反应放出氢气;
D.验纯气体:因为氢气是可燃性气体,进行性质实验之前务必进行验纯,用排水法收集一试管氢气,用拇指堵住,试管口朝下,移近火焰,再移开拇指点火.如果听到尖锐的爆鸣声,则表示氢气不纯,需要重新收集并验纯;如果只听到很微弱的噗噗的声音,则说明氢气已经纯净.
E.收集气体:利用排水法或向下排空气法收集.
F.结束实验:关闭止水夹,产生的氢气无法从导气管中逸出,试管中的气压增大,就会将稀硫酸由分液漏斗下端管口压回分液漏斗中,从而使稀硫酸与锌粒分离,反应停止.
查看习题详情和答案>>
(1)实验原理:通过活泼金属与稀硫酸反应制取氢气通常是用金属
锌
锌
与稀硫酸或稀盐酸
稀硫酸或稀盐酸
反应,若用镁会反应速度太快,不利于收集
反应速度太快,不利于收集
,若用铁会反应速度太慢
反应速度太慢
,若用浓盐酸与锌反应生成氢气,会使制得的氢气中含有氯化氢
氯化氢
气体,可通过氢氧化钠溶液
氢氧化钠溶液
吸收而除去.
(2)反应方程式:
Zn+H2SO4=ZnSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
(3)反应装置如图1( 注意点):
A.长颈漏斗的下端需伸入垫片以下,形成液封,以及有利于固液可以分离.
B.由于氢气难溶于水,密度比空气小,故能用
排水法
排水法
或向上排空气法
向上排空气法
收集.C.优点:可以控制反应的
发生
发生
,停止
停止
;可以节约药品
节约药品
.D.相似的氢气发生装置图2(固液制气,不需加热)
(4)实验步骤
A.按照实验要求,安装好实验仪器;
B.检查仪器装置的气密性:关闭止水夹,向分液漏斗中加入足量的水,若漏斗中的液面能存在一段水柱,并不持续下降,则说明
原装置气密性良好
原装置气密性良好
;C.装药品:先将锌粒放在垫片上,打开止水夹后,向长颈漏斗中注入稀盐酸,发生反应放出氢气;
D.验纯气体:因为氢气是可燃性气体,进行性质实验之前务必进行验纯,用排水法收集一试管氢气,用拇指堵住,试管口朝下,移近火焰,再移开拇指点火.如果听到尖锐的爆鸣声,则表示氢气不纯,需要重新收集并验纯;如果只听到很微弱的噗噗的声音,则说明氢气已经纯净.
E.收集气体:利用排水法或向下排空气法收集.
F.结束实验:关闭止水夹,产生的氢气无法从导气管中逸出,试管中的气压增大,就会将稀硫酸由分液漏斗下端管口压回分液漏斗中,从而使稀硫酸与锌粒分离,反应停止.