摘要:083 mol 0.125 mol 设三种金属的物质的量之和为n.则0.083 mol<n<0.125 mol.故选项C正确. 答案:C
网址:http://m.1010jiajiao.com/timu3_id_72669[举报]
|
T0℃时,在2 L的密闭容器中发生反应:X(g)+Y(g)
| |
A. |
该反应的正反应是吸热反应 |
B. |
T 0℃,从反应开始到平衡时:v(X)=0.083 mol·L-1 min-1 |
C. |
图a中反应达到平衡时,Y的转化率为37.5% |
D. |
T 1℃时,若该反应的平衡常数K=50,则T1<T0 |
已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.30kJ?mol-1,在某温度下2L的密闭容器中进行,测得如下数据:
下列说法正确的是( )
| 时间(h) 物质的量(mol) |
0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | n5 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | n6 |
| NH3 | O | O.20 | n2 | 1.OO | 1.OO |
| A、反应3h内,反应速率秒v(N2)为O.17 mol?L-1?h-1 |
| B、此温度下,该反应的平衡常数为O.037 |
| C、反应进行到1小时时放出的热量为9.23 kJ |
| D、4h时,若再加入1 molN2,达到新的化学平衡时,N2的转化率是原来的两倍 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t1>t2):
|
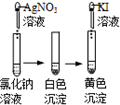
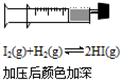
下列事实不能用平衡移动原理解释的是( )
 |
 |
|
| ||||||||||||
| A | B | C | D |
| A、A | B、B | C、C | D、D |
将含1mol HCl的稀盐酸,逐滴加入含0.2mol NaOH和0.5molNa2CO3的混合溶液中,充分反应后溶液中各物质的量是( )
|
查看习题详情和答案>>
