题目内容
已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.30kJ?mol-1,在某温度下2L的密闭容器中进行,测得如下数据:
下列说法正确的是( )
| 时间(h) 物质的量(mol) |
0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | n5 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | n6 |
| NH3 | O | O.20 | n2 | 1.OO | 1.OO |
| A、反应3h内,反应速率秒v(N2)为O.17 mol?L-1?h-1 |
| B、此温度下,该反应的平衡常数为O.037 |
| C、反应进行到1小时时放出的热量为9.23 kJ |
| D、4h时,若再加入1 molN2,达到新的化学平衡时,N2的转化率是原来的两倍 |
分析:A、根据化学平衡三段式列式计算3h生成氨气1mol,消耗氮气0.5mol,依据化学反应速率概念计算分析判断;
B、图表分析可知3h反应达到平衡,依据三段式列式计算平衡浓度,结合平衡常数概念计算;
C、依据反应的焓变结合化学方程式计算放出的热量;
D、加入氮气平衡正向进行,氮气的转化率减小.
B、图表分析可知3h反应达到平衡,依据三段式列式计算平衡浓度,结合平衡常数概念计算;
C、依据反应的焓变结合化学方程式计算放出的热量;
D、加入氮气平衡正向进行,氮气的转化率减小.
解答:解:A、已知合成氨反应,结合平衡三段式列式计算,3h内生成氨气1mol
N2(g)+3H2(g)?2NH3(g)
起始量(mol) 1.5 4.5 0
变化量(mol) 0.5 1.5 1
平衡量(mol) 1 3 1
反应3h内,反应速率v(N2)=
=0.083mol/L?h,故A错误;
B、此温度下,平衡浓度为c(N2)=0.5mol/L,c(H2)=1.5mol/L,c(NH3)=0.5mol/L,该反应的平衡常数K=
=
=O.0148,故B错误;
C、N2(g)+3H2(g)?2NH3(g)△H=-92.30kJ?mol-1,生成2mol氨气放热92.30kJ,反应进行到1小时时,生成氨气0.2mol,放出的热量为9.23 kJ,故C正确;
D、加入氮气平衡正向进行,氮气的转化率减小,故D错误;
故选:C.
N2(g)+3H2(g)?2NH3(g)
起始量(mol) 1.5 4.5 0
变化量(mol) 0.5 1.5 1
平衡量(mol) 1 3 1
反应3h内,反应速率v(N2)=
| ||
| 3h |
B、此温度下,平衡浓度为c(N2)=0.5mol/L,c(H2)=1.5mol/L,c(NH3)=0.5mol/L,该反应的平衡常数K=
| c2(NH3) |
| c(N2)c3(H2) |
| 0.52 |
| 0.5×1.53 |
C、N2(g)+3H2(g)?2NH3(g)△H=-92.30kJ?mol-1,生成2mol氨气放热92.30kJ,反应进行到1小时时,生成氨气0.2mol,放出的热量为9.23 kJ,故C正确;
D、加入氮气平衡正向进行,氮气的转化率减小,故D错误;
故选:C.
点评:本题考查了化学平衡的分析判断,平衡三段式的计算应用,平衡常数,反应热量变化的计算分析,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
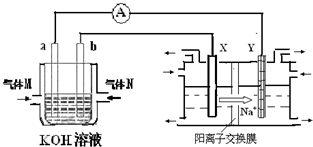 化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.