摘要:下表为元素周期表的一部分.请参照①~⑨在周期表中的位置.回答下列问题. (1)④⑤⑥的原子半径由小到大的顺序是 . (2)②③⑦的最高价含氧酸的酸性由强到弱的顺序是- . (3)写出元素①与元素④按1∶1形成化合物X的化学式 .元素③形成4核10电子化合物Y的化学式是 . (4)中学化学常见物质的转化关系如下: a.将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.红褐色胶体F粒子直径大小的范围为 . b.写出D与Y的水溶液反应的离子方程式: - . c.红棕色G和单质⑨与足量的稀硫酸充分反应.生成FeSO4和H2,Fe2+和H2的质量比为112∶1,若将生成的Fe2+分成4等份.就来源看. 份是来自Fe3+的还原产物. 份是来自H+氧化单质铁的产物.
网址:http://m.1010jiajiao.com/timu3_id_72313[举报]
下表为元素周期表的一部分,回答下列问题:
(1)写出元素符号:①
(2)若用M代表碱金属元素,则其最高价氧化物对应的水化物的化学式为
(3)在元素③与⑩中,化学性质较活泼的是
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
N
N
,④Mg
Mg
,⑥Si
Si
,⑦S
S
.(2)若用M代表碱金属元素,则其最高价氧化物对应的水化物的化学式为
MOH
MOH
;若用X表示卤族元素,则其气态氢化物的分子式为HX
HX
;元素②、⑧、(12)的气态氢化物的稳定性由强到弱的顺序为HF>HCl>HBr
HF>HCl>HBr
(填化学式).(3)在元素③与⑩中,化学性质较活泼的是
K
K
(填元素符号),写出用化学实验证明它较活泼的方法:钾与水的反应比钠与水的反应更剧烈
钾与水的反应比钠与水的反应更剧烈
.下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: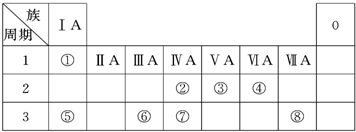
(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式
 .
.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)
a.MnO2 b.CuSO4 c.Na2SO3 d.FeCl3
(5)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应(如图):
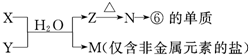
X溶液与Y溶液反应的离子方程式
N→⑥的单质的化学方程式为
M溶液中离子浓度由大到小的排列顺序是
M中阳离子的鉴定方法
查看习题详情和答案>>

(1)地壳中含量居于第二位的元素在周期表中的位置是
第三周期第IVA族
第三周期第IVA族
.(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:
同一主族元素从上到下原子核外电子层数依次增多
同一主族元素从上到下原子核外电子层数依次增多
,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式


(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)
c
c
.a.MnO2 b.CuSO4 c.Na2SO3 d.FeCl3
(5)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3═3H3PO4+H2W↑ |
| 1 | 还原性 还原性 |
H2SO3+Br2+2H2O=H2SO3+2HBr H2SO3+Br2+2H2O=H2SO3+2HBr |
| 2 | 酸性 酸性 |
H2SO3+2NaOH=Na2SO3+2H2O H2SO3+2NaOH=Na2SO3+2H2O |

X溶液与Y溶液反应的离子方程式
Al3++3NH3+3H2O=Al(OH)3↓+3NH4+
Al3++3NH3+3H2O=Al(OH)3↓+3NH4+
,N→⑥的单质的化学方程式为
2Al2O3(熔融)
4Al+3O2↑
| ||
| 冰晶石 |
2Al2O3(熔融)
4Al+3O2↑
,
| ||
| 冰晶石 |
M溶液中离子浓度由大到小的排列顺序是
c(Cl-)>c(NH4+)>c(H+)>c(OH-)或c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)或c(NO3-)>c(NH4+)>c(H+)>c(OH-)
,M中阳离子的鉴定方法
取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子
取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子
.(2009?天津)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)④、⑤、⑥的原子半径由大到小的顺序是
 .
.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 或
或
 或
或 .
.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 C.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
查看习题详情和答案>>

(1)④、⑤、⑥的原子半径由大到小的顺序是
Na>Al>O
Na>Al>O
,⑧的阴离子结构示意图为

(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3>H2SiO3
HNO3>H2CO3>H2SiO3
.(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
 或
或
 或
或
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab
ab
.a.MnO2 b.FeCl3 C.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
,N→⑥的单质的化学方程式为2Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
 4Al+3O2↑
4Al+3O2↑2Al2O3(熔融) 4Al+3O2↑
4Al+3O2↑
,常温下,为使0.1mol/L M溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至 4Al+3O2↑
4Al+3O2↑溶液的pH等于7
溶液的pH等于7
.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑥、⑦的原子半径由小到大的顺序为
(2)②、③、⑧的最高价含氧酸的酸性由弱到强的顺序是
(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,请写出该化合物的电子式
 结构式
结构式
(4)研究表明:②的最高价氧化物在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称
查看习题详情和答案>>
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
O<Si<Al
O<Si<Al
.(2)②、③、⑧的最高价含氧酸的酸性由弱到强的顺序是
H2CO3<HNO3<HClO4
H2CO3<HNO3<HClO4
.(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,请写出该化合物的电子式


H-O-O-H
H-O-O-H
.(4)研究表明:②的最高价氧化物在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称
金刚石
金刚石
、石墨、足球烯或石墨烯
石墨、足球烯或石墨烯
.下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
(1)②的气态氢化物分子的结构式为
 .
.
(2)②、③的最高价含氧酸的酸性由强到弱的顺序是
(3)⑤、⑥元素的金属性强弱依次为
(4)④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式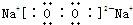
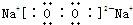 .
.
(5)写出②和⑦中稳定性高的气态氢化物的化学式
(6)用电子式表示⑤和⑨形成化合物的过程:
 .
.
查看习题详情和答案>>
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑨ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |


(2)②、③的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3
HNO3>H2CO3
.(填化学式)(3)⑤、⑥元素的金属性强弱依次为
减小
减小
.(填“增大”、“减小”、或“不变”)(4)④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式
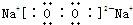
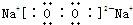
(5)写出②和⑦中稳定性高的气态氢化物的化学式
CH4
CH4
,写出④和⑧中沸点高的气态氢化物的化学式H2O
H2O
,沸点高的理由是水分子间形成氢键
水分子间形成氢键
.(6)用电子式表示⑤和⑨形成化合物的过程:

