网址:http://m.1010jiajiao.com/timu3_id_71764[举报]
 (2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.
(2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:
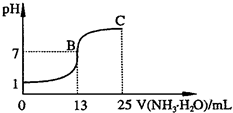
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y.G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl.请推断:①化合物G的化学式为
(2)粉末状G能够与空气中的氧气和水反应,所得的产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料.与氧气反应所得的产物还有一种单质;与水反应生成的另一种产物是该种单质元素的氢化物.请写出化合物G与水反应的化学方程式:
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表达为Si6-xAlxOxN8-x.在接近1700℃时x的极限值约为4.0,在1400℃时x为2.0,以保持整个化合物呈电中性.则赛伦中各元素的化合价为Si
未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机。这类材料中研究得较多的是化合物G。
(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_______________________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
查看习题详情和答案>>(1)化合物G的相对分子质量为140,G中硅元素的质量分数为60%,另有元素Y。G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体。请推断:①化合物G的化学式为__________________。②由1 mol NH3和0.75 mol E恰好完全反应,化合物E的分子式为_______________________。
(2)粉末状G能够与空气中的氧气和水作用,所得产物中都有一种酸性氧化物,它是工业上生产玻璃、水泥、陶瓷的主要原料。与氧反应所得的产物还有一种单质;与水反应生成另一种产物是该种单质元素的氢化物。请写出化合物G与水反应的化学方程式_____________________________________________________________________。
(3)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在G中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品名叫“赛伦”,化学通式可表示为Si6-xAlxOxY8-x。在接近于1 700 ℃时x的极限值约为4.0,在1 400 ℃时x为2.0,以保持整个化合物呈电中性。试问:①赛伦中各元素的化合价为Si_________,Al_________,O_________,Y_________。赛伦的晶体类型为_________。
查看习题详情和答案>>(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:______;
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是______(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)______(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为______;
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式______;
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为______(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用______(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.
 查看习题详情和答案>>
查看习题详情和答案>>