网址:http://m.1010jiajiao.com/timu3_id_69508[举报]
(1)生成氧化亚铜的反应很多,中学化学涉及的反应之一是乙醛与新制的氢氧化铜反应,该反应的化学方程为:
(2)目前常用微乳液-还原法:在100℃,将0.5g十二烷基苯磺酸钠溶解于100mL、0 1mol/L的Cu(NO3)2水溶液中,再快速加入一定体积5mol/L的NaOH水溶液,并搅拌使之混合均匀,再逐滴加入水合肼的水溶液,直至产生红色沉淀,经抽滤、洗涤和真空干燥,得到Cu2O粉末.
①已知:N2H4(l)+O2(g)═N2(g)+2H2O(l)△H=-akJ/mol
Cu(OH)2(s)═CuO(s)+H2O(l)△H=bkJ/mol
4CuO(s)═2Cu2O(s)+O2(g)△H=ckJ/mol
则4Cu(OH)2(s)+N2H4(l)═2Cu2O(s)+N2(g)+6H2O(l)△H=
②十二烷基苯磺酸钠是洗衣粉的主要成分,它在该法中可能的作用是
(3)用铜棒作阳极,钛作阴极,电解氯化钠和氢氧化钠的混合溶液,电解总方程为:2Cu+H2O
| ||
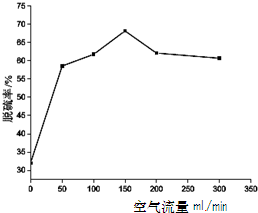
(4)在石化工业中常用纳米Cu2O光解脱硫时,在反应容器中加入一定量含硫混合物[噻吩(C4H4S)和正辛烷按物质的量1:1]并加入0.1g纳米Cu2O,光照同时通入空气1h,分别测定不同流速下最后剩余液中硫的质量分数确定脱硫率,所得结果如右图,下列说法正确的是
A.用正辛烷作溶剂进行实验,是为了模拟柴油的成分
B.用噻吩作含硫化合物是研究有机硫的去除率
C.该实验条件下,空气的流量以150mL/min左右为宜
D.当空气流量超过150mL/min脱硫率下降主要是因为氧化亚铜挥发.
为改善大气质量,国家拟于“十二五”期间,力争将CO2变为燃料或有机化学产品的构想变为现实,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.
Ⅰ.一种将CO2变为燃料或有机化学产品的构想分成3个步骤:
①利用浓碳酸钾溶液吸收空气中的CO2;
②将第①步吸收液电解产生H2和O2,同时分离出CO2;
③将第②步产生的H2(g)和CO2(g)在一定条件下转化成CH4(g)和H2O(l).
已知:H2(g)+![]() O2(g)=H2O(l) ΔH1=-285.8 kJ/mol
O2(g)=H2O(l) ΔH1=-285.8 kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH2=-889.6 kJ/mol
写出第③步反应的热化学方程式为________.
Ⅱ.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.写出甲烷直接将NO2还原得到无污染的产物的化学方程式________.
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)该反应的化学平衡常数表达式为K=________.
在一定温度下,将2 mol NO、1 mol CO充入1 L固定容积的容器中,反应过程中各物质的浓度变化如下图所示.
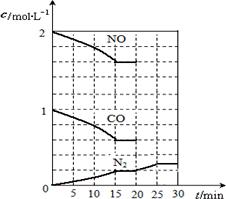
若保持温度不变,20 min时再向容器中充入CO、N2各0.6 mol,平衡将________移动(填“向左”、“向右”或“不”).
若20 min时改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件可能是________(填序号).
①加入催化剂
②降低温度
③缩小容器体积
④增加CO2的量
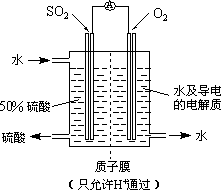
(3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如图,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06 V.实际过程中,将SO2通入电池的________极(填“正”或“负”),负极反应式为________.用这种方法处理SO2废气的优点是可回收大量有效能,副产品为H2SO4,减少环境污染.
I.一种将CO2变为燃料或有机化学产品的构想分成3个步骤:
①利用浓碳酸钾溶液吸收空气中的CO2;
②将第①步吸收液电解产生H2和O2,同时分离出CO2;
③将第②步产生的H2(g)和CO2(g)在一定条件下转化成CH4(g)和H2O(l).
已知:H2(g)+
| 1 |
| 2 |
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2=-889.6kJ/mol
写出第③步反应的热化学方程式为
II.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.写出甲烷直接将NO2还原得到无污染的产物的化学方程式
(2)降低汽车尾气的方法之一是在排气管上安装催化 转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
该反应的化学平衡常数表达式为K=
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图1所示.
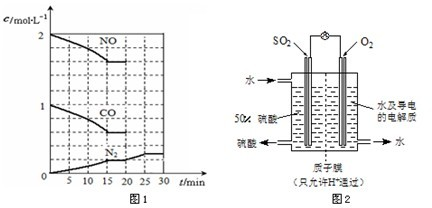
若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
若20min时改变反应条件,导致N2浓度发生如图1所示的变化,则改变的条件可能是
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如图2,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V.实际过程中,将SO2通入电池的
为改善大气质量,国家拟于“十二五”期间,力争将CO2变为燃料或有机化学产品的构想变为现实,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。
I.目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。写出甲烷直接将NO2还原得到无污染的产物的化学方程式 。
(2)降低汽车尾气的方法之一是在排气管上安装催化
转化器,发生如下反应:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。
该反应的化学平衡常数表达式为K= 。
在一定温度下,将2molNO、1molCO充入1L
 固定容积的容器中,反应过程中各物质的浓度变化
固定容积的容器中,反应过程中各物质的浓度变化
如下图所示。
若保持温度不变,20min时再向容器中充入
CO、N2各0.6mol,平衡将 移动(填“向左”、 “向右”或“不”)。
若20min时改变反应条件,导致N2浓度发生如右图所示的变化,则改变的条件可能
是 (填序号)。
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
 (3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如右图,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,写出负极反应式为 。用这种方法处理SO2废气的优点是可回收大量有效能,副产品为H2SO4,减少环境污染。
(3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如右图,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,写出负极反应式为 。用这种方法处理SO2废气的优点是可回收大量有效能,副产品为H2SO4,减少环境污染。
II.有人提出用碳酸钠溶液吸收发电厂废气中的二氧化硫。
已知:H2SO3的电离平衡常数为 K1=1.54×10-2 ,K2=1.O2×10-7
H2CO3的电离平衡常数为K1=4.31×l0-7 K2=5.61×10-11
(4)请写出向碳酸钠溶液中通入一定量的SO2生成无污染的二氧化碳气体的的化学方程式
查看习题详情和答案>>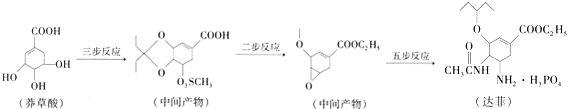
目前世界卫生组织公布的抗流感药物还有扎那米韦,扎那米韦是一种流感病毒神经氨酸酶抑制剂.其结构简式如图所示.请回答下列问题:
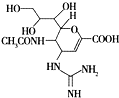
(1)扎那米韦的分子式为______.
(2)写出莽草酸分子中含氧官能团的名称:______.
(3)根据扎那米韦的结构简式推测其不能发生的反应类型是______(填序号,下同).
A.取代反应
B.加成反应
C.酯化反应
D.水解反应
E.硝化反应
(4)下列关于达菲的说法不正确的是______.
①是一种高分子化合物
②在一定条件下能发生水解反应
③既可看成盐,也可看成酯等的多类别物质
④能被新制Cu(OH)2悬浊液氧化
⑤既能使Br2的CCl4溶液褪色,又能使酸性高锰酸钾溶液褪色
⑥分子中含有酯基、肽键、氨基、苯环等结构
(5)已知碳碳双键上连有羟基或一个碳原子上连有两个羟基的结构均不稳定.试写出同时满足以下三个条件的莽草酸的同分异构体的结构简式(任写一种)______.
①含有羧基和碳碳双键 ②羧基直接连在双键的碳原子上 ③含有六元碳环
(6)若将莽草酸与足量乙醇在浓硫酸作用下加热,可以生成分子式为C9H14O5的一种新化合物,该反应的化学方程式为______,反应类型为______.