摘要:2.红磷在Cl2是燃烧.其物质的量之比为1:1.8时.所得产物中PCl3和PCl5的物质的量之比为 A.3:5 B.5:3 C.3:7 D.7:3
网址:http://m.1010jiajiao.com/timu3_id_68329[举报]
红磷在Cl2中燃烧发生的化学反应中,若参加反应的红磷与Cl2的物质的量之比为1:1.8,充分反应后,生成物中PCl5和PCl3的物质的量之比为( )
A.3:5 B.5:3 C.3:7 D.7:3
查看习题详情和答案>>
红磷在Cl2中燃烧发生的化学反应中,若参加反应的红磷与Cl2的物质的量之比为1∶1.8,充分反应后,生成物中PCl5和PCl3的物质的量之比为
A.3∶5
B.5∶3
C.3∶7
D.7∶3
查看习题详情和答案>>
红磷在Cl2中燃烧发生的化学反应中,若参加反应的红磷与Cl2物质的量之比为1∶1.8,充分反应后,生成物PCl5和PCl3的物质的量之比为( )
A.3∶5 B.5∶3 C.3∶7 D.1∶2
查看习题详情和答案>>
红磷在Cl2中燃烧发生的化学反应中,若参加反应的红磷与Cl2的物质的量之比为1:1.8,充分反应后,生成物中PCl5和PCl3的物质的量之比为
- A.3:5
- B.5:3
- C.3:7
- D.7:3
已知PCl3、PCl5在潮湿空气中易发生下列反应,PCl3+3H2O====H3PO3+3HCl,PCl5+4H2O====H3PO4+5HCl。某人设计以下实验为清楚观察到P在Cl2中燃烧分步生成PCl3、PCl5的现象。
先把干燥氯气贮存在100 mL的注射器内,再把火柴头大小的红磷置于玻璃燃烧匙上烘干后组成如图装置。
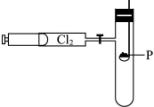
操作分两步进行。首先打开弹簧夹,缓慢推动注射器的针塞,待磷燃烧出现白雾时,立即关闭弹簧夹,停止推入Cl2,片刻后,可见到试管内白雾凝成无色液滴附在试管内壁。然后再打开弹簧夹,继续推入Cl2,就可看到管壁上液滴逐渐消失,管内出现白烟。最后白烟凝结成白色固体附着在试管内壁上。
试完成下列问题:
(1)该实验选择玻璃燃烧匙,不选其他金属燃烧匙的原因是_______________________。
(2)该实验的关键是使用的氯气和红磷必须干燥,其原因是_______________________。
(3)第二次通入氯气时发生反应的化学方程式是_________________________________,推入Cl2之所以要缓慢进行的原因是_________________________________。
查看习题详情和答案>>