网址:http://m.1010jiajiao.com/timu3_id_68081[举报]
| 物质 | 大气中的含量 (体积百分比) |
温室效应 指数 |
| CO2 | 0.03 | 1 |
| H2O | 1 | 0.1 |
| CH4 | 2×10-4 | 30 |
| N2O4 | 3×10-5 | 160 |
| O3 | 4×10-6 | 2000 |
| CCl2F2 | 4.8×10-8 | 25000 |
(1)6种气体中,温室效应指数最大的物质属于
(2)在水分子中,O原子上的价层电子对数为
(3)N2O4分子结构式为
 ,分子为平面结构.N2O4分子中N原子的杂化方式为
,分子为平面结构.N2O4分子中N原子的杂化方式为

(4)O3具有吸收紫外光的功能.
①根据等电子原理,判断O3分子的空间构型为
②紫外光的光子所具有的能量约为399kJ?mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:
| 共价键 | C-C | C-N | C-S |
| 键能/kJ?mol-1 | 347 | 305 | 259 |
(1)1述反应涉及的第三周期元素中,离子半径最小的是______(用元素符号表示).Cl原子与Si原子可以形成的五核分子,其化学键键长和键角都相等,则该物质为______分子(填“极性”或“非极性”),该分子的电子式为______.
(2)不能用于比较Na与Al金属性相对强弱的事实是______.
A.最高价氧化物对应水化物的碱性B.Na和Al的熔点高低
C.单质与H2O反应的难易程度D.比较同浓度NaCl和AlCl3的pH值
(3)1述元素的最高价氧化物对应水化物中,有一种既能与强酸又能与强碱反应,其原因在于:______(用电离方程式表示).
(4)钾长石和烧碱在熔融状态下反应可得到两种正盐,向所得的正盐中加入过量稀盐酸,发生反应的离子方程式分别是:______、______.
(5)制取粗硅的过程中,SiO是反应中间产物,隔绝空气时SiO和NaOH溶液反应(产物之一是硅酸钠)的化学方程式______.
(6)为研究1述反应中钾元素的熔出率(液体中钾元素的质量占全部钾元素质量的百分率)与温度的关系,进行实验(氯化钠与钾长石投料的质量比为2:1),获得如下数据:
时间(h) 钾元素 温度熔出率 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 |
| 830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 |
| 890℃ | 0.579 | 0.691 | 0.694 | 0.699 | 0.699 |
| 950℃ | 0.669 | 0.714 | 0.714 | 0.714 | 0.714 |
②计算890℃时,氯化钠的平衡转化率______(式量:KAlSi3O8-278NaAlSi3O8-262,保留3位小数).
| 元素 性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
| 原子半径 (10-10m) |
1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是
(4)③和⑨两元素比较,非金属性较弱的是
A、气态氢化物的挥发性和稳定性
B、单质分子中的键能
C、两元素的电负性
D、最高价含氧酸的酸性
E、氢化物中X-H键的键长(X代表③和⑨两元素)
F、两单质在自然界的存在形式.
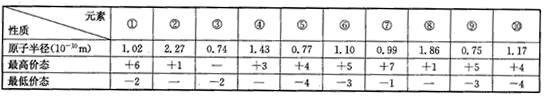
(1)以上10种元素中,第一电离能最小的是__(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8电子稳定结构的物质可能是____(写分子式)。元素⑨和⑩形成的化合物的化学式为_________,它是一种 ____晶体,是重要的结构材料;元素①的原子价电子排布式是____。
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°。三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键——三个原子均等地享有这四个电子,这种特殊的共价键的类型是____键(填“σ”或“π”),在高中化学中有一种常见分子的结合方式与O3相同,它是____(填分子式)。
(4)⑥和⑨两元素比较,非金属性较弱的是____(填名称),可以验证你的结论的是下列中的__________(填序号)。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X-H键的键长(X代表⑥和⑨两元素)
F.两单质在自然界的存在形式
卤族元素的单质和化合物很多,请利用所学物质结构与性质的相关知识回答下列问题:
(1)卤族元素位于周期表的 ????????? 区;氟原子的电子排布图为?????? 溴原子的价电子排布式为????? .
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是??????????
(3)已知高碘酸有两种形式,化学式分别为H5IO6 和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??????????? HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为???????????? 。
和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??????????? HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为???????????? 。
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大。这是由于溶液中发生下列反应 I-+ I2 =I3-与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 ??? 式发生。
A.CsICl2=CsCl+ICl?????? B.CsICl2 =CsI +Cl2
(5)ClO2-的空间构型为?????? 型,中心氯原子的杂化轨道类型为???????? ,写出一个ClO2-的等电子体 ???????????? 。
(6)如图为碘晶体晶胞结构。有关说法中正确的是???? 。

A.碘分子的排列有2种不同的取向
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图)的密度为ρg/cm3 .NA为阿伏加德罗常数,相邻的两个Ca2+核间距为a cm,则CaF2的摩尔质量可以表示为?????? 。
查看习题详情和答案>>