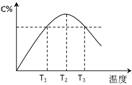
摘要:(2010届无锡市普通高中高三质量调研.11)在某体积固定的密闭容器中进行如下可逆反应:A2C(g).在反应过程中体系的温度持续升高.实验测得混合气体中C的含量与温度关系如图所示.下列说法正确的是 A.此反应的正反应是吸热反应 B.反应在T2温度时达到平衡 C.T3温度时正反应速率大于逆反应速率 D.T3温度时正反应速率大于T1温度时正反应速率
网址:http://m.1010jiajiao.com/timu3_id_66639[举报]
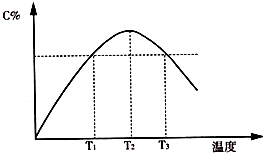 在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中的C的含量与温度关系如图所示.下列说法正确的是( )
在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中的C的含量与温度关系如图所示.下列说法正确的是( )| A、此反应的正反应是吸热反应 | B、反应在T2温度时达到平衡 | C、T2温度时正反应速率大于逆反应速率 | D、T2温度时正反应速率大于T1温度时正反应速率 |
(2013?普陀区二模)研究NO2、SO2、CO等大气污染物的处理具有重要意义.NO2可用下列反应来处理:6NO2(g)+8NH3(g)?7N2(g)+12H2O(g)+Q(Q>0).
完成下列填空:
(1)反应的平衡常数大,处理NO2的效率高.增大该反应平衡常数的措施有
(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是
a.c(NO2):c(NH3)=3:4 b.6v(NO2)=7v(N2)
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若平衡时NO2和N2的浓度之比为m/n,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比
(4)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测得刚好有3mol电子发生转移,则在2分钟内NH3的平均反应速率为:v(NH3)=
查看习题详情和答案>>
完成下列填空:
(1)反应的平衡常数大,处理NO2的效率高.增大该反应平衡常数的措施有
降低温度
降低温度
.(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是
c
c
.a.c(NO2):c(NH3)=3:4 b.6v(NO2)=7v(N2)
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若平衡时NO2和N2的浓度之比为m/n,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比
>
>
m/n(填“>”、“=”或“<”).(4)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测得刚好有3mol电子发生转移,则在2分钟内NH3的平均反应速率为:v(NH3)=
0.25mol/(L?min)
0.25mol/(L?min)
.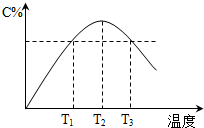 在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示.下列说法正确的是( )
在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示.下列说法正确的是( )| A、此反应的正反应是吸热反应 | B、反应在T2温度时达到平衡 | C、T3温度时正反应速率大于逆反应速率 | D、T3温度时正反应速率大于T1温度时正反应速率 |
研究NO2 、SO2 、CO等大气污染物的处理具有重要意义。NO2可用下列反应来处理:
6 NO2(g)+8NH3(g) 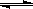 7N2(g)+12H2O(g)+Q(Q>0)。
7N2(g)+12H2O(g)+Q(Q>0)。
完成下列填空:
(1)反应的平衡常数大,处理NO2的效率高。增大该反应平衡常数的措施有 。
(2)一定条件下上述反应在某体积固定的密闭容器中进行,能说明该反应已经达到平衡状态的是 。
a.c(NO2):c(NH3) = 3:4 b.6v(NO2) = 7v(N2)
c.容器内气体总压强不再变化 d.容器内气体密度不再变化
(3)若平衡时NO2和N2的浓度之比为m/n,保持其它条件不变,缩小反应容器的体积后达到新的平衡,此时NO2和N2的浓度之比 m/n(填“>”、“=”或“<”)。
(4)某温度下,在一个容积为2升的反应容器内,上述反应2分钟后达到平衡,测得刚好有3mol电子发生转移,则在2分钟内NH3的平均反应速率为:
v(NH3) = 。
查看习题详情和答案>>
 2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示。下列说法正确的是
2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示。下列说法正确的是