摘要:9.A.B.C三种强电解质.它们在水中电离出的离子如下表所示: 阳离子 Na+.K+.Cu2+ 阴离子 SO42- .OH- 下图所示装置中.甲.乙.丙三个烧杯依次分别盛放足量的A溶液.足量的B溶液.足量的C溶液.电极均为石墨电极. 接通电源.经过一段时间后.测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系图如上.据此回答下列问题: (1)M为电源的 极 电极b上发生的电极反应为 , (2)计算电极e上生成的气体在标准状态下的体积: , (3)写出乙烧杯的电解池反应 (4)如果电解过程中B溶液中的金属离子全部析出.此时电解能否继续进行.为什么? . (5)若经过一段时间后.测得乙中c电极质量增加了16g.要使丙恢复到原来的状态.操作是
网址:http://m.1010jiajiao.com/timu3_id_64404[举报]
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
如图所示装置中,甲、乙、丙三个烧杯分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图.据此回答下列问题:
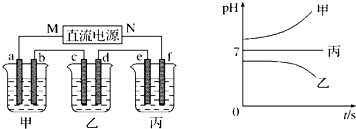
(1)M为电源的
(2)计算电极e上生成的气体在标准状况下的体积
(3)写出乙烧杯中发生电解的总反应化学方程式
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行
(5)此时要使丙中溶液恢复到原来的状态,操作是
查看习题详情和答案>>
| 阳离子 | Na+、K+、Cu2+ | ||
| 阴离子 | SO
|

(1)M为电源的
负
负
极(填写“正”或“负”);电极b上发生的电极反应式为4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
.(2)计算电极e上生成的气体在标准状况下的体积
5.6L
5.6L
.(3)写出乙烧杯中发生电解的总反应化学方程式
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
.
| ||
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行
能
能
(填写“能”或“否”)原因为电解硫酸溶液
电解硫酸溶液
.(5)此时要使丙中溶液恢复到原来的状态,操作是
加入4.5g水
加入4.5g水
.A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.
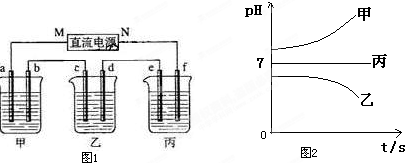
接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系图如图2.据此回答下列问题:
(1)M为电源的
(2)写出乙烧杯的电解反应方程式
(3)计算电极e上生成的气体在标准状态下的体积
(4)要使丙恢复到原来的状态,需要加入一种
查看习题详情和答案>>
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |

接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系图如图2.据此回答下列问题:
(1)M为电源的
负
负
极(填写“正”或“负”);电极b上发生的电极反应为4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
;(2)写出乙烧杯的电解反应方程式
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
;
| ||
(3)计算电极e上生成的气体在标准状态下的体积
5.6L
5.6L
;(4)要使丙恢复到原来的状态,需要加入一种
水
水
物质4.5
4.5
克.A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极.
接通电源,经过一段时间后,测得乙中C电极质量增加了27克.常温下各烧杯中溶液的pH与电解时间t的关系图如图1.据此回答下列问题:

(1)M为电源的
(2)写出甲烧杯中反应的化学方程式
(3)有人设想用图2所示原电池为直流电源完成上述电解.则锌电极相当于直流电源的
(4)有人设想用图3所示装置做直流电源,不仅可以完成电解也能将气体SO2 转化为重要化工原料.该设想中负极的电极反应式为
查看习题详情和答案>>
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
接通电源,经过一段时间后,测得乙中C电极质量增加了27克.常温下各烧杯中溶液的pH与电解时间t的关系图如图1.据此回答下列问题:

(1)M为电源的
负
负
极(填“正”或“负”);甲、乙电解质分别为NaCl
NaCl
、AgNO3
AgNO3
(填化学式).(2)写出甲烧杯中反应的化学方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(3)有人设想用图2所示原电池为直流电源完成上述电解.则锌电极相当于直流电源的
M
M
(填“M”或“N”)极.(4)有人设想用图3所示装置做直流电源,不仅可以完成电解也能将气体SO2 转化为重要化工原料.该设想中负极的电极反应式为
SO2+2H2O-2e-═4H++SO42-
SO2+2H2O-2e-═4H++SO42-
.A、B、C三种强电解质,它们在水中电离出的离子如表所示:
 |
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42— 、OH- |
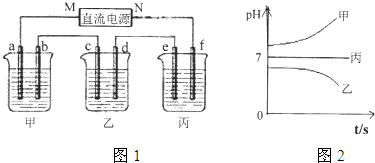
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。
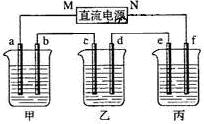
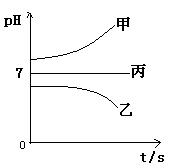
接通电源,经过一段时间后,测得乙中c电极质量增加了16g。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”)
电极b上发生的电极反应为 ;
(2)计算电极e上生成的气体在标准状态下的体积: ;
(3)写出乙烧杯的电解池反应
(4)若经过一段时间后,测得乙中c电极质量增加了16g,要使丙恢复到原来的状态,操作是
查看习题详情和答案>>