摘要:氯碱厂电解饱和食盐水制取NaOH的工艺流程如下: (粗盐中杂质离子为:SO42- .Mg2+ .Ca2+) (1)精制过程中反应的离子方程式为 . (2)电解过程的总反应方程式为 . (3)电解槽阳极产物可用于 . (4)已知NaOH.NaCl在水中的溶解度数据如下表: 温度/℃ 20 30 40 50 60 70 80 90 100 NaOH /g 109 118 129 146 177 300 313 318 337 NaCl/ g 36 36.3 36.6 37 37.3 37.8 38.4 39 39.8 根据上述数据.脱盐的主要工序应为 . .脱盐后的碱液含NaOH约50%.含NaCl仅约2%左右.NaCl能够从溶液中大量析出的原因是 .
网址:http://m.1010jiajiao.com/timu3_id_64380[举报]
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图1所示.
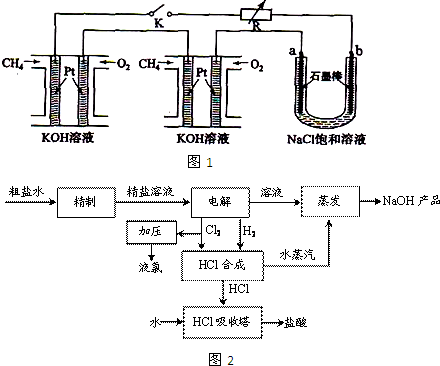
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
(2)闭合K开关后,a、b电极上均有气体产生.电解氯化钠溶液的总反应方程式为
(3)氯碱厂电解饱和食盐水制取烧碱,同时制盐酸的工艺流程如图2:
根据题意完成下列填空:
①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A 盐酸;B BaCl2溶液;C NaOH溶液;D Na2CO3溶液.加入试剂的顺序是
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
③HCl合成反应中保持过量的气体是
④利用HCl合成时放出的热量来产生水蒸汽,用于NaOH溶液的蒸发,这样做的优点是
⑤检验NaOH产品中是否含有NaCl的实验方案是
查看习题详情和答案>>

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
2O2+4H2O+8e-=8OH-
2O2+4H2O+8e-=8OH-
、CH4+10OH--8e-=CO32-+7H2O
CH4+10OH--8e-=CO32-+7H2O
.(2)闭合K开关后,a、b电极上均有气体产生.电解氯化钠溶液的总反应方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
;
| ||
(3)氯碱厂电解饱和食盐水制取烧碱,同时制盐酸的工艺流程如图2:
根据题意完成下列填空:
①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A 盐酸;B BaCl2溶液;C NaOH溶液;D Na2CO3溶液.加入试剂的顺序是
BCDA或CBDA
BCDA或CBDA
.②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
2Cl--2e→Cl2
2Cl--2e→Cl2
.与电源负极线连的电极附近溶液pH变大
变大
(变大、不变、变小).③HCl合成反应中保持过量的气体是
氢气
氢气
;从HCl合成塔的观察口能观察到的现象是苍白色火焰
苍白色火焰
.④利用HCl合成时放出的热量来产生水蒸汽,用于NaOH溶液的蒸发,这样做的优点是
充分利用能量
充分利用能量
.⑤检验NaOH产品中是否含有NaCl的实验方案是
加足量稀硝酸至呈酸性,然后滴加硝酸银溶液,若产生白色沉淀,则含有氯化钠
加足量稀硝酸至呈酸性,然后滴加硝酸银溶液,若产生白色沉淀,则含有氯化钠
.(2011?大连模拟)氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程示意图如下所示,完成下列填空:
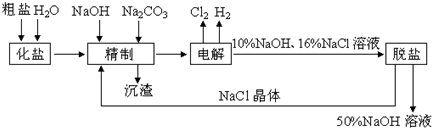
(1)在电解过程中,与电源正极相连的电极上电极反应为
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂不能是
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为了有效除去Ca2+、Mg2+、SO42-,加入试剂不合理的顺序为
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
查看习题详情和答案>>

(1)在电解过程中,与电源正极相连的电极上电极反应为
2Cl--2e-═Cl2↑
2Cl--2e-═Cl2↑
,与电源负极相连的电极附近,溶液pH升高
升高
(选填“不变”、“升高”或“下降”).(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为
Ca2++CO32-═CaCO3↓、Mg2++2OH-═Mg(OH)2↓
Ca2++CO32-═CaCO3↓、Mg2++2OH-═Mg(OH)2↓
.(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂不能是
b
b
.a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为了有效除去Ca2+、Mg2+、SO42-,加入试剂不合理的顺序为
a
a
(选填a、b、c)a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
加热蒸发
加热蒸发
、冷却、过滤
过滤
(填写操作名称)除去NaCl.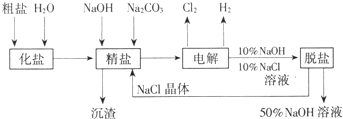 氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图:
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图:依据图,完成下列填空:
(1)电解饱和食盐水所发生的化学反应方程式为
(2)若对10L饱和食盐水电解两分钟共收集标准状况下的气体22.4L,电解后溶液的pH=
(3)为有效除去粗盐中含有的Ca2+、Mg2+、SO42-,加入试剂的合理顺序可以是
A.先加NaOH,后加Na2CO3,再加BaCl2,最后用盐酸酸化
B.先加NaOH,后加BaCl2,再加Na2CO3,最后用盐酸酸化
C.先加BaCl2,后加NaOH,再加Na2CO3,最后用盐酸酸化
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
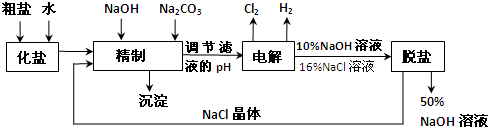
依据上图完成下列问题:
(1)在电解过程中,阴极上生成气体的电子式为 .
(2)精制过程中除去阳离子中的Ca2+、Mg2+等杂质,除去Mg2+的离子方程式为 .
(3)精制过程要除去SO42-,可选择下列溶液中的 (填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图上(精制过程中加入试剂从左到右的顺序为先后顺序).
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)在实际生产中也可以用BaCO3除去SO42-(已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释: .
(5)脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、 (填操作名称)而制得50%的NaOH溶液.
查看习题详情和答案>>

依据上图完成下列问题:
(1)在电解过程中,阴极上生成气体的电子式为
(2)精制过程中除去阳离子中的Ca2+、Mg2+等杂质,除去Mg2+的离子方程式为
(3)精制过程要除去SO42-,可选择下列溶液中的
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)在实际生产中也可以用BaCO3除去SO42-(已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释:
(5)脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、
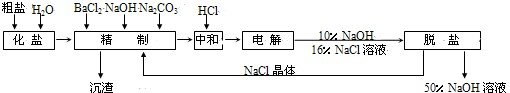 (2009?广州模拟)氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:
(2009?广州模拟)氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:(1)精制过程中反应的离子方程式为
Ba2++SO42-=BaSO4↓,Mg2++2OH-=Mg(OH)2↓,Ca2++CO32-=CaCO3↓,Ba2++CO32-=BaCO3↓
Ba2++SO42-=BaSO4↓,Mg2++2OH-=Mg(OH)2↓,Ca2++CO32-=CaCO3↓,Ba2++CO32-=BaCO3↓
.(2)电解过程的总反应方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(3)电解槽阳极产物可用于
制漂白粉、生产盐酸、自来水消毒、制高纯硅、合成塑料等(任写2种)
制漂白粉、生产盐酸、自来水消毒、制高纯硅、合成塑料等(任写2种)
(至少写出两种用途).(4)已知NaOH、NaCl在水中的溶解度数据如下表:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaOH/g | 109 | 118 | 129 | 146 | 177 | 300 | 313 | 318 | 337 |
| NaCl/g | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
蒸发
蒸发
、浓缩
浓缩
.脱盐后的碱液含NaOH约50%,含NaCl仅约2%左右,NaCl能够从溶液中大量析出的原因是蒸发过程中溶剂(水)大量减少,Na+浓度显著增加促进NaCl的沉淀溶解平衡向沉淀方向移动(或:Na+浓度显著增加抑止了NaCl的溶解)
蒸发过程中溶剂(水)大量减少,Na+浓度显著增加促进NaCl的沉淀溶解平衡向沉淀方向移动(或:Na+浓度显著增加抑止了NaCl的溶解)
.