网址:http://m.1010jiajiao.com/timu3_id_64300[举报]
有以下6种物质,结合相关问题填空:
①Al ②FeCl3溶液 ③SO2 ④碱石灰 ⑤液氨 ⑥NaOH固体
(1)能导电的是 ;属于非电解质的是
(2)碱石灰常用作干燥剂,其不能干燥下列 气体(以上各空用相关编号填写)
A.H2 B.NH3 C.CO2 D.O2
(3)①与⑥溶液反应的产物中Al的化合价为 价;其反应的化学方程式为:_________________________________________________________
(4)向②溶液中加入KI溶液后,用CCl4萃取,CCl4层呈紫色,写出该反应过程的离子方程式:________________________________________
查看习题详情和答案>>(11分)有以下6种物质,结合相关问题填空:
①Al ②FeCl3溶液 ③SO2 ④碱石灰 ⑤液氨 ⑥NaOH固体
(1)能导电的是 ;属于非电解质的是
(2)碱石灰常用作干燥剂,其不能干燥下列 气体(以上各空用相关编号填写)
A.H2 B.NH3 C.CO2 D.O2
(3)①与⑥溶液反应的产物中Al的化合价为 价;其反应的化学方程式为:_________________________________________________________
(4)向②溶液中加入KI溶液后,用CCl4萃取,CCl4层呈紫色,写出该反应过程的离子方程式:________________________________________
查看习题详情和答案>>有以下8种物质,结合相关问题填空:
①Cu ②FeCl3溶液 ③FeCl2溶液 ④碱石灰 ⑤液氨 ⑥NaCl固体 ⑦ 稀硫酸 ⑧SO2
⑨Na2O2固体
⑴能导电的是 ;属于电解质的是 ;属于非电解质的是 。
⑵碱石灰常用作干燥剂,它不能干燥下列 气体
A.H2 B.NH3 C.Cl2 D.O2 E.SO2
⑶向②溶液中加入KI溶液后,用CCl4萃取,CCl4层呈紫色,写出该反应过程的离子方程式:
⑷写出Na2O2与CO2反应的化学方程式并表示出电子转移的方向和数目
查看习题详情和答案>>
①Al ②FeCl3溶液 ③SO2 ④碱石灰 ⑤液氨 ⑥NaOH固体
(1)能导电的是___________;属于非电解质的是___________
(2)碱石灰常用作干燥剂,其不能干燥下列___________气体(以上各空用相关编号填写)
A.H2 B.NH3 C.CO2 D.O2
(3)①与⑥溶液反应的产物中Al的化合价为___________价;其反应的化学方程式为:______________________________
(4)向②溶液中加入KI溶液后,用CCl4萃取,CCl4层呈紫色,写出该反应过程的离子方程式:
________________________________
(9分)pH=12的NaOH溶液100ml,要使它的pH为11。(体积变化忽略不计)
(1)如果加入蒸馏水,应加 mL。
(2)如果加入pH=10的NaOH溶液,就加 mL。
(3)如果加0.01mol/L的HC1,应加 mL。
【解析】考查pH的计算。
(1)若加水稀释。强碱每稀释10n倍,强碱的pH就减小n个单位,pH由12变为11,则相当于稀释10倍,及最终溶液的体积是1000ml,所以需要水1000ml-100ml=900ml。
(2)若加入强碱。PH=11,则混合后OH-的物质的量浓度为0.001mol/L。所以有 ,解得V=1L.
,解得V=1L.
(3)若加入盐酸,则发生中和反应。因此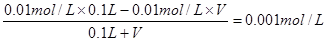 ,解得V=0.0818L。
,解得V=0.0818L。
查看习题详情和答案>>