摘要:10.H2CO3和H2S在25℃时的电离常数如下: 电离常数 Ka1 Ka2 H2CO3 4.2×10-7 5.6×10-11 H2S 5.7×10-8 1.2×10-15 则下列判断正确的是 A. NaHCO3+NaHS=Na2CO3+H2S反应可能发生 B. H2S+Na2CO3=NaHS+NaHCO3 反应不可能发生 C. 将Na2S溶液适当加热.溶液中阴离子数目会增多 D. Na2CO3溶液中:C(Na+)+C(H+)=C(CO32-)+ C(HCO3-)+C(OH-)
网址:http://m.1010jiajiao.com/timu3_id_63119[举报]
|
H2CO3和H2S在25℃时的电离常数如下:
则下列反应可能发生的是 | |
| [ ] | |
A. |
NaHCO3+NaHS→Na2CO3+H2S |
B. |
H2S+Na2CO3→NaHS+NaHCO3 |
C. |
Na2S+H2O+CO2→Na2CO3+H2S |
D. |
H2S+NaHCO3→NaHS+H2CO3 |
H2CO3和H2S在25℃时的电离常数如下:
| 电离常数 | Ki1 | Ki2 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
| H2S | 5.7×10-8 | 1.2×10-15 |
则下列反应可能发生的是
A. NaHCO3+NaHS=Na2CO3+H2S B. H2S+2Na2CO3=Na2S+2NaHCO3
C. Na2S+H2O+CO2=NaHS+NaHCO3 D. H2S+NaHCO3=NaHS+H2CO3
查看习题详情和答案>>
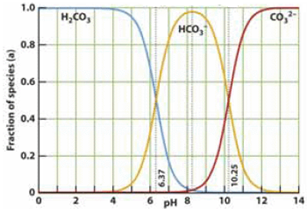 如图是一水溶液在pH从 0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是
如图是一水溶液在pH从 0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是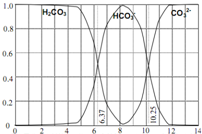 如图是一水溶液在pH从0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是( )
如图是一水溶液在pH从0至14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成百分率,下列叙述正确的是( )