摘要:X.Y.Z.W均为短周期元素.X.Y同主族.X元素的原子有2个电子层.每层上均有2个电子,Z处于第2周期第ⅤA族,W元素是地壳中质量分数第2的元素.其单质是现代信息技术中应用的重要材料之一.下列叙述正确的是( ) A.X.Y最高价氧化物对应水化物的碱性相比.X>Y B.X元素的原子半径比Z元素原子半径小 C.Z元素的非金属性一定比W元素的非金属性强 D.Z的单质不能助燃.因此Y的单质在Z的单质中不能燃烧
网址:http://m.1010jiajiao.com/timu3_id_62998[举报]
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法不正确的是( )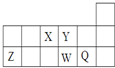

| A、离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+) | B、若存在简单阴离子R2-,则R不一定与Y、W同主族 | C、元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 | D、X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个。下列叙述正确的是
A.原子半径Z>W>Y>X
B.Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应
C.气态氢化物的稳定性Z>W
D.X的气态氢化物与足量W单质在光照条件下反应生成物均为气体
查看习题详情和答案>>
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是

A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)> r(Z3+)
B.若存在简单阴离子R2-,则R不一定与Y、W同主族
C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
查看习题详情和答案>>