网址:http://m.1010jiajiao.com/timu3_id_61242[举报]
①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;?
③B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;?
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。?
请填写下列空白:?
(1)D2C2的电子式 。?
(2)1 mol E单质与足量乙的溶液反应,能生产 mol A2气体。并写出其反应的离子方程式 。
(3)写出下列溶液反应的离子方程式:?
乙+丙: 。?
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为 。?
(5)以石墨为电极,电解乙的溶液400 mL,当电路中通过a mol电子时,阴、阳两极共产生气体 L(标准状况),溶液中c (OH-) (填“增大”“减小”或“不变”)。
查看习题详情和答案>>①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;?
③B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;?
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。
请填写下列空白:?
(1)D2C2的电子式 。?
(2)1 mol E单质与足量乙的溶液反应,能生产 mol A2气体。并写出其反应的离子方程式 。
(3)写出下列溶液反应的离子方程式:?
乙+丙: 。?
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为 。?
(5)以石墨为电极,电解乙的溶液400 mL,当电路中通过a mol电子时,阴、阳两极共产生气体 L(标准状况),溶液中c(OH-) (填“增大”“减小”或“不变”)。?
查看习题详情和答案>>①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小
②A、D同主族,A是所有元素中原子半径最小的元素
③B、D、E三者的最高价氧化物的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和
请填写下列空白:
(1)A
(2)单质F与足量乙的溶液反应的离子方程式为___________,1 mol单质E与乙溶液完全反应时,产生__________mol A2气体。
(3)写出乙+丙在溶液中反应的离子方程式___________________________________________。
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为:______________________________________________________________。
(5)以石墨为电极,电解乙的溶液
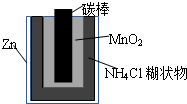 Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH4Cl混合溶液.(1)该电池的负极材料是
(2)如果该电池的工作原理为:Zn+2NH4Cl=ZnCl2+2NH3+H2,其正极反应式为:
(3)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀.其主要原因是
a.NaOH b.Zn c.Fe d.NH3?H2O
(4)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是:
(1)该电池的负极材料是
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀.其主要原因是
a.NaOH b.Zn c.Fe d.NH3?H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是: