摘要:没有自由移动离子参加反应.不能写离子方程式
网址:http://m.1010jiajiao.com/timu3_id_60879[举报]
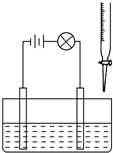 在烧杯里加入20mL 0.1mol?L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):
在烧杯里加入20mL 0.1mol?L-1的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):实验现象如下:
①灯泡逐渐变暗;②烧杯中有白色沉淀生成,溶液红色变浅甚至消失.请依据实验现象回答下列问题:
(1)灯泡变暗的原因是
溶液中可自由移动离子的浓度变小
溶液中可自由移动离子的浓度变小
.(2)有白色沉淀生成,说明
Ba2+与SO42-发生了反应
Ba2+与SO42-发生了反应
,红色变浅说明发生了H+与OH-发生了反应,使溶液碱性减弱
发生了H+与OH-发生了反应,使溶液碱性减弱
.(3)当Ba2+恰好完全沉淀时,消耗NaHSO4溶液的体积为
20
20
mL,溶液呈浅红
浅红
色,离子反应方程式为Ba2++OH-+SO42-+H+═BaSO4↓+H2O
Ba2++OH-+SO42-+H+═BaSO4↓+H2O
.(4)若向(3)得到的溶液中,继续滴加NaHSO4溶液到恰好变为无色,此阶段的离子反应方程式为
H++OH-═H2O
H++OH-═H2O
.下列说法正确的是( )
| A、SO2的水溶液能导电,说明SO2是电解质 | B、Ksp小的物质不可能转化为Ksp大的物质 | C、在水溶液中能电离出自由移动离子的晶体不一定是离子晶体 | D、2NO+2CO?2CO2+N2 的△H<0,则该反应一定能自发进行 |
 CO2+N2 的△H<0,则该反应一定能自发进行
CO2+N2 的△H<0,则该反应一定能自发进行