摘要:答案 (1)Fe + 2Fe3+ = 3Fe2+ (2)加入硫酸.H+浓度增大.使Fe2+ + 2H2OFe(OH)2 + 2H+的平衡向逆反应方向移动.从而抑制FeSO4的水解 (3)Fe2+ + 2HCO3- = FeCO3↓+ CO2 ↑ + H2O 4FeCO3 + 6H2O + O2 = 4Fe(OH)3 ↓+ 4CO2 (4)取少量洗涤后的滤液放入试管中.滴加酸化的BaCl2溶液.若无白色沉淀产生.则沉淀洗涤干净 (5)288.0
网址:http://m.1010jiajiao.com/timu3_id_59852[举报]
15年前,清华才女朱令离奇铊中毒的事件曾引发一场多年难解的疑案.而在近日,广东东莞一名在电子企业打工的女工也意外出现铊中毒并被家属认为是“职业病”,因而再度引发各方关注.铊(Tl)盐与氰化钾(KCN)被列为A级危险品.已知下列反应在一定条件下能够发生:(1)Tl3++2Ag═Tl++2Ag+,(2)Ag++Fe2+═Ag+Fe3+,(3)Fe+2Fe3+═3Fe2+,下列离子氧化性的比较正确的是( )
查看习题详情和答案>>
(2009?海淀区一模)现有中学化学常见的物质X、Y、甲、乙、丙、丁,它们之间的反应关系为(反应条件略去):
①单质X+化合物甲→单质Y+化合物乙;②单质Y+化合物丙→化合物丁.请针对以下不同情况回答:
(1)若乙为有磁性的化合物,反应①的化学方程式是
(2)若X、Y为不同金属,甲为红棕色固体,工业上常用电解乙来制取X,X阳离子的结构示意图为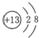
 ,反应②的离子方程式是
,反应②的离子方程式是
(3)若X、Y为不同主族非金属气态单质,甲常温下呈液态,丁溶于水形成的溶液呈强酸性,则X的化学式是
(4)除上述给定的情况外,请再写出一组同时符合反应①、②转化关系的化学方程式.
反应①:
反应②:
查看习题详情和答案>>
①单质X+化合物甲→单质Y+化合物乙;②单质Y+化合物丙→化合物丁.请针对以下不同情况回答:
(1)若乙为有磁性的化合物,反应①的化学方程式是
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
.
| ||
(2)若X、Y为不同金属,甲为红棕色固体,工业上常用电解乙来制取X,X阳离子的结构示意图为


Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
.(3)若X、Y为不同主族非金属气态单质,甲常温下呈液态,丁溶于水形成的溶液呈强酸性,则X的化学式是
F2
F2
,反应②的化学方程式是2SO2+O2
2SO3或2NO+O2=2NO2
| ||
| 高温高压 |
2SO2+O2
2SO3或2NO+O2=2NO2
.
| ||
| 高温高压 |
(4)除上述给定的情况外,请再写出一组同时符合反应①、②转化关系的化学方程式.
反应①:
C+H2O═CO+H2或Fe+HCl=FeCl2+H2↑
C+H2O═CO+H2或Fe+HCl=FeCl2+H2↑
反应②:
H2+CH3CHO═CH3CH2OH
H2+CH3CHO═CH3CH2OH
.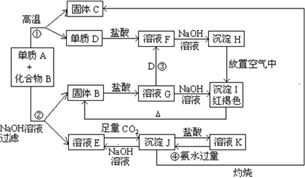 由单质A与化合物B两种粉末组成的混合物,在一定条件下可按如图所示发生转化:
由单质A与化合物B两种粉末组成的混合物,在一定条件下可按如图所示发生转化:请回答:
(1)A的化学式
Al
Al
; B的化学式Fe2O3
Fe2O3
(2)反应①的化学方程式
2Al+Fe2O3
2Fe+Al2O3
| ||
. |
2Al+Fe2O3
2Fe+Al2O3
| ||
. |
(3)反应②的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)反应③的离子方程式
Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
(5)反应④的离子方程式
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
.(1)物质的量各为1mol的钠、镁、铝与1mol?L-1的盐酸100mL反应,在相同条件下产生氢气的体积之比是
(2)除去FeCl2溶液中少量的FeCl3最好加入
(3)鉴别Na2CO3和NaHCO3溶液可选用
(4)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是
①NaAlO2 ②(NH4)2CO3 ③Na2CO3 ④Al(OH)3 ⑤Ca(OH)2 ⑥NaHSO3.
查看习题详情和答案>>
10:1:1
10:1:1
.等物质的量的Na2CO3和NaHCO3与足量的盐酸反应,在相同条件下产生二氧化碳的体积之比是1:1
1:1
.(2)除去FeCl2溶液中少量的FeCl3最好加入
Fe
Fe
物质,离子方程式为Fe+2Fe3+═3Fe2+
Fe+2Fe3+═3Fe2+
.除去SO2气体中少量的HCl最好加入饱和NaHSO3溶液
饱和NaHSO3溶液
物质,离子方程式为HSO3-+H+═SO2↑+H2O
HSO3-+H+═SO2↑+H2O
.(3)鉴别Na2CO3和NaHCO3溶液可选用
①③
①③
.(填序号)①CaCl2 ②Ca(OH)2 ③BaCl2(4)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是
②④⑥
②④⑥
.(填序号)①NaAlO2 ②(NH4)2CO3 ③Na2CO3 ④Al(OH)3 ⑤Ca(OH)2 ⑥NaHSO3.
(1)下列装置1能组装成原电池的是

(2)对于锌-铜-稀硫酸组成的原电池装置,当导线中有0.1mol电子通过时,写出负极的电池反应式
(3)如图2所示装置:若烧杯中溶液为氢氧化钠溶液,则负极为
(4)利用反应:Fe+2Fe3+=3Fe2+设计一个化学电池(电极材料和电解液自选),画出实验装置图3,注明电解质溶液名称和正负极材料.
查看习题详情和答案>>
I、Ⅲ
I、Ⅲ
.(填序号)
(2)对于锌-铜-稀硫酸组成的原电池装置,当导线中有0.1mol电子通过时,写出负极的电池反应式
Zn-2e-=Zn2+
Zn-2e-=Zn2+
,铜片上析出1.12L
1.12L
LH2(标准状况下).(3)如图2所示装置:若烧杯中溶液为氢氧化钠溶液,则负极为
Al
Al
,总反应方程为2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.(4)利用反应:Fe+2Fe3+=3Fe2+设计一个化学电池(电极材料和电解液自选),画出实验装置图3,注明电解质溶液名称和正负极材料.