摘要:溶液浅绿色溶液---FeCl2 溶液.FeSO4 溶液.Fe(NO3)2 溶液黄色溶液---FeCl3 溶液.Fe2(SO4)3 溶液.Fe(NO3)3 溶液蓝色溶液---CuCl2 溶液.CuSO4 溶液.Cu(NO3)2 溶液蓝绿色溶液-CuCl2 溶液
网址:http://m.1010jiajiao.com/timu3_id_5886[举报]
(2013?香洲区模拟)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉.脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)
(1)Fe(OH)2读作
(2)某同学自制脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行如下两个实验:
实验Ⅰ:

请回答:
乙在净水中用作
实验Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如下图(部分产物略去).

①金属B的化学式是
②区别溶液C与溶液D物质的方法是
③反应③的化学方程式为:
查看习题详情和答案>>
(1)Fe(OH)2读作
氢氧化亚铁
氢氧化亚铁
;此反应的基本类型是化合反应
化合反应
.(2)某同学自制脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行如下两个实验:
实验Ⅰ:

请回答:
乙在净水中用作
吸附剂
吸附剂
;溶液丙中含有的溶质是FeSO4、NaCl、H2SO4
FeSO4、NaCl、H2SO4
(写化学式).实验Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如下图(部分产物略去).

①金属B的化学式是
Cu
Cu
②区别溶液C与溶液D物质的方法是
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
;③反应③的化学方程式为:
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
.(2011?成都)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉.脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)
(1)Fe(OH)2读作
(2)某同学自制脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行如下两个实验:
实验Ⅰ:

请回答:操作Ⅰ的名称是
溶液丙中含有的溶质是
实验Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如下图(部分产物略去).
①反应①的条件是
②金属A与B的活动性:A
③区别溶液C与溶液D物质的方法是
④反应③的化学方程式为:
查看习题详情和答案>>
(1)Fe(OH)2读作
氢氧化亚铁
氢氧化亚铁
;此反应的基本类型是化合反应
化合反应
.(2)某同学自制脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行如下两个实验:
实验Ⅰ:

请回答:操作Ⅰ的名称是
过滤
过滤
,乙在净水中用作吸附剂
吸附剂
;溶液丙中含有的溶质是
FeSO4、NaCl、H2SO4
FeSO4、NaCl、H2SO4
(写化学式)实验Ⅱ:将乙烘干后进行如下实验,物质之间的转化关系如下图(部分产物略去).

①反应①的条件是
高温
高温
;②金属A与B的活动性:A
>
>
B(填“>”“<”或“﹦”);③区别溶液C与溶液D物质的方法是
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
;④反应③的化学方程式为:
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
,向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为CuSO4+BaCl2=BaSO4↓+CuCl2
CuSO4+BaCl2=BaSO4↓+CuCl2
.常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉.
脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)
(1)Fe(OH)2读作
(2)某同学用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行两个实验:
实验Ⅰ:
请回答:
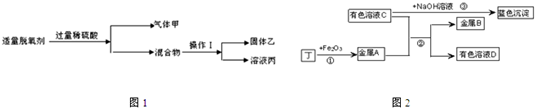
如图1,①操作Ⅰ的名称是
②溶液丙中含有的金属阳离子是
实验Ⅱ:将乙洗涤烘干后,二氧化碳通过灼热的乙生成丁.进行如图2实验,物质之间的转化关系如图(部分产物略去).
①金属A与B的活动性:A
②区别有色溶液C与有色溶液D的方法是
③反应①的化学方程式为:
④向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为
查看习题详情和答案>>
脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 (红褐色固体)

(1)Fe(OH)2读作
氢氧化亚铁
氢氧化亚铁
.(2)某同学用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g食盐)进行两个实验:
实验Ⅰ:
请回答:
如图1,①操作Ⅰ的名称是
过滤
过滤
;②溶液丙中含有的金属阳离子是
Fe2+、Na+
Fe2+、Na+
(写微粒符号)实验Ⅱ:将乙洗涤烘干后,二氧化碳通过灼热的乙生成丁.进行如图2实验,物质之间的转化关系如图(部分产物略去).
①金属A与B的活动性:A
>
>
B(填“>”“<”或“﹦”);②区别有色溶液C与有色溶液D的方法是
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
观察溶液颜色,浅绿色为FeSO4溶液,蓝色为CuSO4溶液
;③反应①的化学方程式为:
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
;
| ||
④向溶液C中加入BaCl2溶液,有白色沉淀产生.其化学方程式为
CuSO4+BaCl2=BaSO4↓+CuCl2
CuSO4+BaCl2=BaSO4↓+CuCl2
.12、享受生活离不开化学知识,家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.
(1)米、面的主要成分属于六大营养素中的
(2)液态的植物油和固态的动物脂肪合称为油脂,若锅里的油着火了,可采取的灭火措施是
(3)厨房中常见的盐主要有食盐和纯碱,若要区分食盐和纯碱,请你选用一种简便、可行的方法是
(4)白糖与红糖主要成分都是蔗糖.利用活性炭的
(5)随着科技的进步,食品防腐技术也在不断发展.亚硝酸钠(NaNO3)是一种常用的防腐剂.结合下图“小资料”回答问题:
①亚硝酸钠属于
②食品添加亚硝酸钠的量要严加控制,我国规定肉类灌肠中,亚硝酸钠的最高添加标准为150mg/kg,以此计算,100g30%的亚硝酸钠溶液至少可用于生产肉灌肠
③针对资料,小明设计如图实验:实验A中的化学方程式为
④亚硝酸钠加热分解放出有刺激性气味的气体,该气体可能是
A.NO2 B.NH3 C.N2 D.SO2.
查看习题详情和答案>>

(1)米、面的主要成分属于六大营养素中的
糖类
;(2)液态的植物油和固态的动物脂肪合称为油脂,若锅里的油着火了,可采取的灭火措施是
盖锅盖,隔绝空气
;(3)厨房中常见的盐主要有食盐和纯碱,若要区分食盐和纯碱,请你选用一种简便、可行的方法是
品尝,有咸味的是食盐,有涩味的是纯碱;加食醋,有气泡产生的原物质是纯碱,无明显现象的是食盐(其他正确答案也可)
;(4)白糖与红糖主要成分都是蔗糖.利用活性炭的
吸附
性,可将红糖脱色成白糖;(5)随着科技的进步,食品防腐技术也在不断发展.亚硝酸钠(NaNO3)是一种常用的防腐剂.结合下图“小资料”回答问题:
①亚硝酸钠属于
盐
(选填“酸、碱、盐或氧化物”);②食品添加亚硝酸钠的量要严加控制,我国规定肉类灌肠中,亚硝酸钠的最高添加标准为150mg/kg,以此计算,100g30%的亚硝酸钠溶液至少可用于生产肉灌肠
200
千克.③针对资料,小明设计如图实验:实验A中的化学方程式为
Fe+2HCl=FeCl2+H2↑
;实验B观察到溶液由浅绿色变为黄色,小红设计上述实验的目的是探究亚硝酸钠能否将二价铁转化三价铁
;④亚硝酸钠加热分解放出有刺激性气味的气体,该气体可能是
A
(填字母).A.NO2 B.NH3 C.N2 D.SO2.
(2007?连云港)某研究性学习小组在综合实践活动中对某化工厂化验室排出的废水感兴趣,并对其进行了探究:
[调查获悉]废水中含有硝酸亚铁、硝酸银
[查阅资料]含硝酸亚铁的溶液呈浅绿色
[实验目的]探究用锌从废水中最大程度地回收金属银的方法;探究锌和废水中硝酸亚铁、硝酸银的反应顺序
[实验用品]废水、所需化学试剂及相关的仪器、用品
[设计方案]他们设计了如下方案:
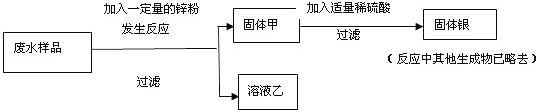
[发现问题]小组成员分别进行实验,在得到固体甲的同时发现:有些同学得到无色溶液乙,有些同学得到深浅不同的浅绿色溶液乙,小丹同学提出问题:哪种结果能最大程度地回收金属银呢?锌与废水中哪种物质先反应呢?
[讨论分析]小军同学认为:这个问题必须通过探究溶液乙或固体甲的组成才能回答,此观点得到了大家的赞同,经研究,他们决定探究溶液乙.于是他们分成两小组,第一组对无色溶液进行探究,第二组对浅绿色溶液进行探究:
(1)首先他们对溶液乙中的溶质作出了多种猜想:
第一组:①溶质为 Zn(NO3)2 ②溶质为 Zn(NO3)2、AgNO3
第二组:③溶质为 Fe(NO3)2和
(2)小悦同学思考后指出:“通过实验或推理,都能排除第一组同学提出的猜想②,从而确立猜想①是合理的”,请你叙述其推理过程
.
(3)第二组同学经过向不同的浅绿色溶液中加入一种试剂,观察实验现象后得出结论,使③④两种猜想都得以验证.请你参与到实验操作过程中并完成下表:
[交流后得出结论]
(4)当反应后溶液呈无色,溶质为
[探究后反思](5)老师评价:这种方法虽然方便、快捷,但也有不足,请你指出它的不足
查看习题详情和答案>>
[调查获悉]废水中含有硝酸亚铁、硝酸银
[查阅资料]含硝酸亚铁的溶液呈浅绿色
[实验目的]探究用锌从废水中最大程度地回收金属银的方法;探究锌和废水中硝酸亚铁、硝酸银的反应顺序
[实验用品]废水、所需化学试剂及相关的仪器、用品
[设计方案]他们设计了如下方案:

[发现问题]小组成员分别进行实验,在得到固体甲的同时发现:有些同学得到无色溶液乙,有些同学得到深浅不同的浅绿色溶液乙,小丹同学提出问题:哪种结果能最大程度地回收金属银呢?锌与废水中哪种物质先反应呢?
[讨论分析]小军同学认为:这个问题必须通过探究溶液乙或固体甲的组成才能回答,此观点得到了大家的赞同,经研究,他们决定探究溶液乙.于是他们分成两小组,第一组对无色溶液进行探究,第二组对浅绿色溶液进行探究:
(1)首先他们对溶液乙中的溶质作出了多种猜想:
第一组:①溶质为 Zn(NO3)2 ②溶质为 Zn(NO3)2、AgNO3
第二组:③溶质为 Fe(NO3)2和
Zn(NO3)
Zn(NO3)
④溶质为 Fe(NO3)2、Zn(NO3)2
Zn(NO3)2
和AgNO3
AgNO3
(2)小悦同学思考后指出:“通过实验或推理,都能排除第一组同学提出的猜想②,从而确立猜想①是合理的”,请你叙述其推理过程
若猜想②成立,说明Fe(NO3)2与Zn反应生成Fe,而Fe会与过滤前的溶液中AgNO3反应,即铁和AgNO3不可能都有,从而排除猜想②
若猜想②成立,说明Fe(NO3)2与Zn反应生成Fe,而Fe会与过滤前的溶液中AgNO3反应,即铁和AgNO3不可能都有,从而排除猜想②
.
(3)第二组同学经过向不同的浅绿色溶液中加入一种试剂,观察实验现象后得出结论,使③④两种猜想都得以验证.请你参与到实验操作过程中并完成下表:
| 实验操作 | 实验现象和结论 |
| 取少量乙溶液于试管中, 在溶液中插入一根铜丝 在溶液中插入一根铜丝 ,观察.或者(取少量乙溶液于试管中, 滴加几滴稀盐酸(或其他氯化物溶液) 滴加几滴稀盐酸(或其他氯化物溶液) ) | 若 铜丝表面无变化 铜丝表面无变化 ,则是Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2 ,若铜丝表面有银白色固体析出 铜丝表面有银白色固体析出 则是Zn(NO3)2、Fe(NO3)2、AgNO3 Zn(NO3)2、Fe(NO3)2、AgNO3 .或者(若 溶液无明显变化 溶液无明显变化 ,则溶质是Zn(NO3)2、Fe(NO3)2 Zn(NO3)2、Fe(NO3)2 ,若溶液中有沉淀生成 溶液中有沉淀生成 ,则溶质是Zn(NO3)2、Fe(NO3)2、AgNO3 Zn(NO3)2、Fe(NO3)2、AgNO3 .) |
(4)当反应后溶液呈无色,溶质为
Zn(NO3)2
Zn(NO3)2
或当反应后溶液呈浅绿色,溶质为Zn(NO3)2
Zn(NO3)2
和Fe(NO3)2
Fe(NO3)2
时,能最大程度地回收金属银.通过探究,同学们认为:“使用过量的锌,过滤后得无色溶液”是方便、快捷并确保最大程度地回收金属银的一种方法.经过观察和思考,同学们还得出了 Zn先和废水中AgNO3
AgNO3
反应,再和Fe(NO3)2
Fe(NO3)2
反应的结论.[探究后反思](5)老师评价:这种方法虽然方便、快捷,但也有不足,请你指出它的不足
浪费一些锌和稀硫酸,最好能对亚铁盐和锌盐进行回收利用,又能减少污染(或其他合理答案)
浪费一些锌和稀硫酸,最好能对亚铁盐和锌盐进行回收利用,又能减少污染(或其他合理答案)
.