摘要:(1)2H2O+O2+4e-==?4OH-.CO2+2OH-==CO23-+H2O.2H2-4e-==?4H+.2H+CO23-==?CO2↑+H2O(2)阴极.4OH--4e-?==2H2O+O2↑(3)生成甲烷可作飞船的燃料.使呼吸产生的废气二氧化碳得到充分利用.体现了原子经济的原则.
网址:http://m.1010jiajiao.com/timu3_id_58294[举报]
菜刀上沾有食盐水后,置于空气中一段时间会生锈,其原理是( )
|
查看习题详情和答案>>
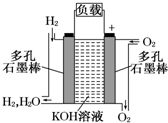 (1)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
(1)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:①图中通过负载的电子流动方向
向右
向右
(填“向左”或“向右”).②写出氢氧燃料电池工作时电极反应方程式
正极:
2H2O+O2+4e-═4OH-
2H2O+O2+4e-═4OH-
,负极:
2H2+4OH--4e-═4H2O
2H2+4OH--4e-═4H2O
,(2)在由铜片、锌片和200ml稀硫酸组成的原电池中,若H2只在铜片上产生,当在铜片上放出4.48L(标准状况)的H2时,硫酸恰好用完,则产生这些气体消耗的锌为
13
13
g,在导线上有0.4
0.4
mol电子通过,原稀硫酸的物质的量浓度是1mol/L
1mol/L
.金属是人类生产、生活中不可缺少的重要材料
(1)生铁是
(2)生铁放置在潮湿的空气发生电化学腐蚀时的正极反应为
(3)下列对金属制品采取的防护方法不正确的是
①在电线的外面包上一层塑料层
②在自行车钢圈上镀上一层金属铬
③在海轮的铁制外壳上焊上铜块
④在铁制的暖气片上刷一层油漆.
查看习题详情和答案>>
(1)生铁是
C
C
(填化学式)和铁的合金,生铁的硬度比纯铁高
高
(填高、低).(2)生铁放置在潮湿的空气发生电化学腐蚀时的正极反应为
2H2O+O2+4e-=4OH-
2H2O+O2+4e-=4OH-
;负极反应为Fe-2e-=Fe2+
Fe-2e-=Fe2+
;用盐酸可以除去生铁表面的铁锈,该反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O
Fe2O3+6H+=2Fe3++3H2O
.(3)下列对金属制品采取的防护方法不正确的是
③
③
(填序号).①在电线的外面包上一层塑料层
②在自行车钢圈上镀上一层金属铬
③在海轮的铁制外壳上焊上铜块
④在铁制的暖气片上刷一层油漆.