摘要:6.解建立计算模式: X + 2Y 2Z n始(mol) a b 0 Δn(mol) x 2x 2x n平(mol) a-x b-2x 2x 据题意:mol=2xmol mol 气体Y的转化率= 故B项正确.
网址:http://m.1010jiajiao.com/timu3_id_57334[举报]
【选考-物质结构与性质】
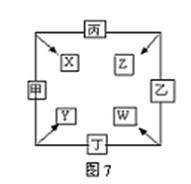
Q、X、W、Y、Z都是元素周期表中前36号的元素,其中X、W同周期,Q、W同主族,已知:
①电负性Q>W;X、Y原子的价层电子构型为nS1,其电离能数据如下:
②X、Y、Z可与W形成XW、YW、ZW化合物,YW中阳离子与阴离子电子层结构相同,ZW中阳离子的最外层3d轨道无单电子.
回答下列问题:
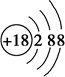
(1)写出Q元素原子的轨道表示式为 .
(2)比较XW、YW的熔点高低并说明理由. .
(3)写出Z的价层电子排布式 ;灼烧化合物ZW2火焰发出绿色的光,请用原子结构的知识解释发光原因 .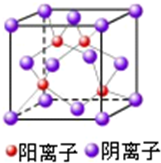
(4)ZW的晶胞结构如图所示,阴离子周围最近的阳离子有 个;ZW晶体的密度为a g?cm-3,则晶胞的体积是 (只要求列出计算式).
(5)Q的气态氢化物在25℃、80℃及90℃(均在常压下),测得其摩尔质量分别为58.0g/mol、20.6g/mol、20.0g/mol.在不同温度下摩尔质量不同的可能原因 .
查看习题详情和答案>>
Q、X、W、Y、Z都是元素周期表中前36号的元素,其中X、W同周期,Q、W同主族,已知:
①电负性Q>W;X、Y原子的价层电子构型为nS1,其电离能数据如下:
| X | Y | |
| 第一电离能(KJ/mol) | 495.8 | 418.8 |
回答下列问题:
(1)写出Q元素原子的轨道表示式为
(2)比较XW、YW的熔点高低并说明理由.
(3)写出Z的价层电子排布式

(4)ZW的晶胞结构如图所示,阴离子周围最近的阳离子有
(5)Q的气态氢化物在25℃、80℃及90℃(均在常压下),测得其摩尔质量分别为58.0g/mol、20.6g/mol、20.0g/mol.在不同温度下摩尔质量不同的可能原因
通常把具有相同电子数和相同原子数的分子或离子称为等电子体。等电子体的结构和性质相似(等电子原理)。有下列两个系列的物质:
系列一:CH4 C2H6 CO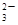 Y C2O
Y C2O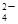 W
W
系列二:NH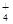 N2H
N2H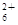 X NO
X NO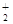 Z N2
Z N2
试根据等电子体的概念及上述两系列物质的排列规律,推断X、Y、Z、W可能是下列各组物质中的( )
A.NO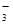 CO2 N2O4 CO
CO2 N2O4 CO
B.NO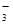 CO2 N2H4 C2H2
CO2 N2H4 C2H2
C.NO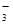 CO NO
CO NO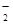 C2H2
C2H2
D.NO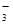 HCO
HCO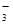 N2O
N2O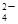 CO
CO
查看习题详情和答案>>
 X ②
X ②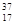 X ③
X ③  ④
④