摘要:A 2.AD 3.A 讲析:1.核外电子数=核内质子数=118 ,核内中子数与核外电子数之差:175-118=57 2.相对分子质量为70的分子是由两个35C1原子构成的.相对分子质量为72的是由一个35C1和一个37Cl原子构成的.相对分子质量为74的分子是由两个37C1原子构成的.由此可以计算出每个选项中分子数比对应的35Cl与37C1原子个数比值. 3.题给信息只能推知该同位素原子的质量数.因此选项B错误,未指明哪种碳的同位素.选项C错误,m.n的数值不确定.故选项D也错误.
网址:http://m.1010jiajiao.com/timu3_id_56823[举报]
下表列出了A~R 9种元素在周期表中的位置
用元素符号填写下空:
(1)这9中元素中金属性最强的是
(2)化学性质最不活泼的元素是
(3)G的最高价含氧酸的化学式是
(4)E的最简单氢化物的化学式
(5)A在F中燃烧得到产物的化学式
(6)C与D的原子半径比较:R(C)
查看习题详情和答案>>
| 周期族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)这9中元素中金属性最强的是
K
K
;(2)化学性质最不活泼的元素是
Ar
Ar
;(3)G的最高价含氧酸的化学式是
HClO4
HClO4
;(4)E的最简单氢化物的化学式
CH4
CH4
;(5)A在F中燃烧得到产物的化学式
Na2O2
Na2O2
;(6)C与D的原子半径比较:R(C)
>
>
R(D)(填“>”或“<”)下表列出了九种元素在元素周期表中的位置:
根据题意,用元素符号或化学式填空:
(1)这几种元素中,金属性最强的是
(2)G元素和H元素的核电荷数之差是
(3)A、B、C三种元素的原子半径由大到小的顺序为
(4)用电子式表示H元素跟A元素形成化合物的过程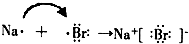
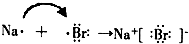 .
.
(5)C、D两元素比较,金属性较强的是
①将在空气中放置已久的C和D的单质分别与热水反应
②将除去氧化物薄膜的C与D的单质分别和热水作用,并滴入酚酞溶液
③将除去氧化物薄膜的C与D的单质分别和2mL1mol?L-1的盐酸反应
④比较这两种元素的气态氢化物的稳定性
(6)D和F两种元素形成的化合物与强碱反应的离子方程式为
查看习题详情和答案>>
族 周期 |
I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)这几种元素中,金属性最强的是
K
K
;化学性质最不活泼的是Ar
Ar
.(2)G元素和H元素的核电荷数之差是
18
18
;含有6个中子的E原子的化学符号为126C
126C
.(3)A、B、C三种元素的原子半径由大到小的顺序为
K>Na>Mg
K>Na>Mg
.(4)用电子式表示H元素跟A元素形成化合物的过程
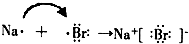
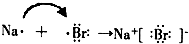
(5)C、D两元素比较,金属性较强的是
Mg
Mg
,可以验证该结论的实验是②③
②③
(用编号表示).①将在空气中放置已久的C和D的单质分别与热水反应
②将除去氧化物薄膜的C与D的单质分别和热水作用,并滴入酚酞溶液
③将除去氧化物薄膜的C与D的单质分别和2mL1mol?L-1的盐酸反应
④比较这两种元素的气态氢化物的稳定性
(6)D和F两种元素形成的化合物与强碱反应的离子方程式为
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.下表列出了A-R9种元素在周期表中的位置,用元素符号或化学式填空.
(1)这九种元素中:化学性质最不活泼的是 ;金属性最强的是: 最高价氧化物的水化物碱性最强的碱的电子式是 最高价氧化物的水化物酸性最强的酸是 ;
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应的水化物反应的离子方程式是 .
(3)A、B、C三种元素按原子半径由大到小的顺序排列的为 .
(4)F的氢化物的电子式 ;G、H氢化物的稳定性递减的顺序是: .
(5)H元素跟A元素形成的化合物的电子式是 .
(6)C和G两种元素形成的化合物属于 (填“离子化合物”或“共价化合物”),请用电子式表示其形成过程 .
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应的水化物反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列的为
(4)F的氢化物的电子式
(5)H元素跟A元素形成的化合物的电子式是
(6)C和G两种元素形成的化合物属于
下表是元素周期表的一部分,根据下表用元素符号或化学式填空:
(1)这九种元素分别为A
F
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)写出F元素的氢化物在常温下跟B元素的单质发生反应的化学方程式并标出电子转移的方向和数目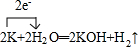
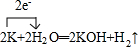 .
.
(5)H元素跟A元素形成化合物的电子式是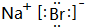
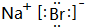 .高温灼烧该化合物时,火焰呈
.高温灼烧该化合物时,火焰呈
(6)H元素和G元素两者核电荷数之差是
查看习题详情和答案>>
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
Na
Na
、BK
K
、CMg
Mg
、DAl
Al
、EC
C
、F
O
O
、GCl
Cl
、HBr
Br
、RAr
Ar
,其中化学性质最不活泼的是Ar
Ar
.(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是
NaOH
NaOH
.(3)A、B、C三种元素按原子半径由大到小的顺序排列为
K+>Na+>Mg2+
K+>Na+>Mg2+
.(4)写出F元素的氢化物在常温下跟B元素的单质发生反应的化学方程式并标出电子转移的方向和数目
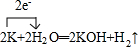
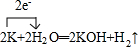
(5)H元素跟A元素形成化合物的电子式是
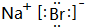
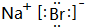
黄
黄
色.(6)H元素和G元素两者核电荷数之差是
18
18
.(13分)下表列出了A—R9种元素在周期表中的位置,用元素符号或化学式填空。
|
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
E |
|
F |
|
|
|
3 |
A |
C |
D |
|
|
|
G |
R |
|
4 |
B |
|
|
|
|
|
H |
|
(1)这九种元素中:化学性质最不活泼的是 ;金属性最强的是: 最高价氧化物的水化物碱性最强的碱的电子式是 最高价氧化物的水化物酸性最强的酸是 ;
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(2分) 。
(3 )A、B、C三种元素按原子半径由大到小的顺序排列的为 。
(4)F的氢化物的电子式 ;G、H 氢化物的稳定性递减的顺序是: 。
(5)H元素跟A元素形成的化合物的电子式是 。
(6 ) C和G两种元素形成的化合物属于 (填“离子化合物”或“共价化合物”),请用电子式表示其形成过程(2分) 。
查看习题详情和答案>>
 主族 周期
主族 周期