摘要:20.某兴趣小组利用如图所示的装置进行二氧化碳的制取和部分性质的实验.请回答下列问题:(1)关闭E.打开C.从长颈漏斗 中加入 与锥形瓶B中的 固体接触.即有二氧化碳 气体产生.有关反应的化学方程式是 观察到D中的蜡烛慢慢熄灭.说明二氧 化碳具有 的性质. (2)关闭C.打开E.观察到G中的蜡烛燃烧得更旺.说明有 生成. 查阅资料:二氧化碳能与过氧化钠(Na2O2)反应生成碳酸钠和氧气. 该反应的化学方程式是 . [实验探究]要检验反应后F中的固体物质中含有碳酸钠.可取少量反应后的F中的固体物质于试管中.滴入 .观察到气泡产生.用蘸有澄清石灰水的玻璃片放在试管口.可观察到 .写出有关反应的化学方程式 . .
网址:http://m.1010jiajiao.com/timu3_id_5642[举报]
某兴趣小组利用下图所示的实验装置进行化学实验探究活动,请你参与他们的活动,并回答有关的问题:

[查资料](1)、碳酸氢钠(NaHCO3)加热分解产物是碳酸钠、二氧化碳以及水.
(2)、分液漏斗可以通过活塞控制液体的滴加速度.
[设计实验](1)、小红同学利用过氧化氢溶液中加入MnO2(固体粉末)来制取氧气,用这种方法制取氧气时,你认为应选用的发生装置是 (填序号),请你告诉小红同学你选用该装置的理由: ,应选用的收集装置是: .
(2)、小方同学认为上述发生装置制取时有优点:(请你写出一点) .
(3)、小玲同学通过查阅资料,得知:制取二氧化碳气体除了实验室常用大理石与稀盐酸外,还可以加热固体碳酸氢钠的方法来制取,请写出反应的化学方程式: .收集二氧化碳气体的装置是: .要在规定的时间内顺利完成实验,小组成员之间应: .
[实验结论]实验室制取气体时,应根据反应的原理和反应条件以及所制气体的有关性质来选择实验发生装置和收集装置.
[交流与反思]在第3个实验中要证明仍有少量反应物NaHCO3未完全分解,应进行如下的实验:
查看习题详情和答案>>

[查资料](1)、碳酸氢钠(NaHCO3)加热分解产物是碳酸钠、二氧化碳以及水.
(2)、分液漏斗可以通过活塞控制液体的滴加速度.
[设计实验](1)、小红同学利用过氧化氢溶液中加入MnO2(固体粉末)来制取氧气,用这种方法制取氧气时,你认为应选用的发生装置是
(2)、小方同学认为上述发生装置制取时有优点:(请你写出一点)
(3)、小玲同学通过查阅资料,得知:制取二氧化碳气体除了实验室常用大理石与稀盐酸外,还可以加热固体碳酸氢钠的方法来制取,请写出反应的化学方程式:
[实验结论]实验室制取气体时,应根据反应的原理和反应条件以及所制气体的有关性质来选择实验发生装置和收集装置.
[交流与反思]在第3个实验中要证明仍有少量反应物NaHCO3未完全分解,应进行如下的实验:
| 所用装置以及操作方法 | 实验现象 | 解释与结论 |
| 将装置A与F相连并加热剩余的反应物 | F中的现象:_______________ | 结论:____________ F中的反应化学方程:_____ |
某兴趣小组利用下图所示的实验装置进行化学实验探究活动,请你参与他们的活动,并回答有关的问题:
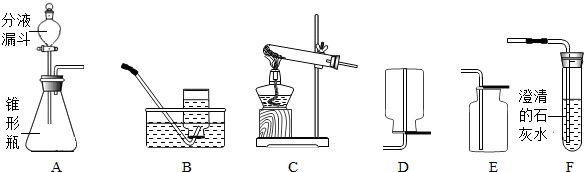
[查资料](1)、碳酸氢钠(NaHCO3)加热分解产物是碳酸钠、二氧化碳以及水.
(2)、分液漏斗可以通过活塞控制液体的滴加速度.
[设计实验](1)、小红同学利用过氧化氢溶液中加入MnO2(固体粉末)来制取氧气,用这种方法制取氧气时,你认为应选用的发生装置是______(填序号),请你告诉小红同学你选用该装置的理由:______,应选用的收集装置是:______.
(2)、小方同学认为上述发生装置制取时有优点:(请你写出一点)______.
(3)、小玲同学通过查阅资料,得知:制取二氧化碳气体除了实验室常用大理石与稀盐酸外,还可以加热固体碳酸氢钠的方法来制取,请写出反应的化学方程式:______.收集二氧化碳气体的装置是:______.要在规定的时间内顺利完成实验,小组成员之间应:______.
[实验结论]实验室制取气体时,应根据反应的原理和反应条件以及所制气体的有关性质来选择实验发生装置和收集装置.
[交流与反思]在第3个实验中要证明仍有少量反应物NaHCO3未完全分解,应进行如下的实验:
| 所用装置以及操作方法 | 实验现象 | 解释与结论 |
| 将装置A与F相连并加热剩余的反应物 | F中的现象:_______________ | 结论:____________ F中的反应化学方程:_____ |
某兴趣小组利用下图所示的实验装置进行化学实验探究活动,请你参与他们的活动,并回答有关的问题:
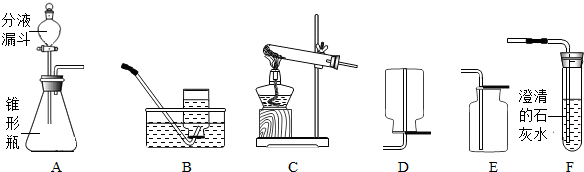
[查资料](1)、碳酸氢钠(NaHCO3)加热分解产物是碳酸钠、二氧化碳以及水.
(2)、分液漏斗可以通过活塞控制液体的滴加速度.
[设计实验](1)、小红同学利用过氧化氢溶液中加入MnO2(固体粉末)来制取氧气,用这种方法制取氧气时,你认为应选用的发生装置是______(填序号),请你告诉小红同学你选用该装置的理由:______,应选用的收集装置是:______.
(2)、小方同学认为上述发生装置制取时有优点:(请你写出一点)______.
(3)、小玲同学通过查阅资料,得知:制取二氧化碳气体除了实验室常用大理石与稀盐酸外,还可以加热固体碳酸氢钠的方法来制取,请写出反应的化学方程式:______.收集二氧化碳气体的装置是:______.要在规定的时间内顺利完成实验,小组成员之间应:______.
[实验结论]实验室制取气体时,应根据反应的原理和反应条件以及所制气体的有关性质来选择实验发生装置和收集装置.
[交流与反思]在第3个实验中要证明仍有少量反应物NaHCO3未完全分解,应进行如下的实验:
查看习题详情和答案>>

[查资料](1)、碳酸氢钠(NaHCO3)加热分解产物是碳酸钠、二氧化碳以及水.
(2)、分液漏斗可以通过活塞控制液体的滴加速度.
[设计实验](1)、小红同学利用过氧化氢溶液中加入MnO2(固体粉末)来制取氧气,用这种方法制取氧气时,你认为应选用的发生装置是______(填序号),请你告诉小红同学你选用该装置的理由:______,应选用的收集装置是:______.
(2)、小方同学认为上述发生装置制取时有优点:(请你写出一点)______.
(3)、小玲同学通过查阅资料,得知:制取二氧化碳气体除了实验室常用大理石与稀盐酸外,还可以加热固体碳酸氢钠的方法来制取,请写出反应的化学方程式:______.收集二氧化碳气体的装置是:______.要在规定的时间内顺利完成实验,小组成员之间应:______.
[实验结论]实验室制取气体时,应根据反应的原理和反应条件以及所制气体的有关性质来选择实验发生装置和收集装置.
[交流与反思]在第3个实验中要证明仍有少量反应物NaHCO3未完全分解,应进行如下的实验:
| 所用装置以及操作方法 | 实验现象 | 解释与结论 |
| 将装置A与F相连并加热剩余的反应物 | F中的现象:_______________ | 结论:____________ F中的反应化学方程:_____ |
某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答:

(1))在图中写出标数字的仪器名称:①
(2)若用加热高锰酸钾来制取并收集较干燥的氧气,应选用的制取和收集装置是
(3)用双氧水和二氧化锰制取氧气时,应该选用的发生装置是
(4)实验室制取二氧化碳,选用的药品是
(5)加热铜绿应选择
(6)联想:氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气.氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.制取氨气应选择
查看习题详情和答案>>

(1))在图中写出标数字的仪器名称:①
分液漏斗
分液漏斗
②锥形瓶
锥形瓶
(2)若用加热高锰酸钾来制取并收集较干燥的氧气,应选用的制取和收集装置是
AC
AC
(填装置序号),反应的表达式为高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
,若用E装置收集氧气,水槽中出现紫红色,最可能的原因是| 加热 |
试管口未放棉花
试管口未放棉花
;实验结束时,应该先将导管从水槽中移出
将导管从水槽中移出
,后熄灭酒精灯
熄灭酒精灯
,目的为了防止水倒吸引起试管炸裂
防止水倒吸引起试管炸裂
.若用E装置收集O2,应在气泡连续、均匀冒出
气泡连续、均匀冒出
时开始收集;若用C装置收集O2,验满的方法是将带火星的木条放于瓶口,若木条复燃则满
将带火星的木条放于瓶口,若木条复燃则满
.(3)用双氧水和二氧化锰制取氧气时,应该选用的发生装置是
B
B
(填装置序号),反应文字表达式为过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
.若反应很剧烈,据此提出实验安全注意事项是| 二氧化锰 |
①
①
(填序号)①控制液体的滴加速度②用体积较小的反应容器③加热反应物(4)实验室制取二氧化碳,选用的药品是
大理石或石灰石
大理石或石灰石
和稀盐酸
稀盐酸
(填名称),反应的表达式是碳酸钙+盐酸→氯化钙+水+二氧化碳
碳酸钙+盐酸→氯化钙+水+二氧化碳
.若用C装置收集CO2,验满的方法是将燃烧的木条放于瓶口,若木条熄灭则满
将燃烧的木条放于瓶口,若木条熄灭则满
.为了得到二氧化碳气体,甲、乙两个化学兴趣小组分别设计了如上图所示的F发生装置.你认为可行吗?不可行
不可行
,若不合理,应如何改正?长颈漏斗下端伸入液面以下
长颈漏斗下端伸入液面以下
.(5)加热铜绿应选择
A
A
装置进行实验(填装置序号),反应表达式为碱式碳酸铜
氧化铜+二氧化碳+水
| 加热 |
碱式碳酸铜
氧化铜+二氧化碳+水
.若实验结束发现试管破裂的原因可能是| 加热 |
试管口高于试管底部(合理均可)
试管口高于试管底部(合理均可)
(写出一种可能的原因).(6)联想:氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气.氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.制取氨气应选择
A和D
A和D
装置(填装置序号).请写出氨气和氧化铜(CuO)反应的表达式氨气+氧化铜
铜+水+氮气
| 加热 |
氨气+氧化铜
铜+水+氮气
.| 加热 |
 某兴趣小组利用废旧电话线中的金属铜丝进行了如下一系列实验.
某兴趣小组利用废旧电话线中的金属铜丝进行了如下一系列实验.(1)如图所示,将铜丝分别放入盛有氯化锌溶液、稀硫酸、硝酸银溶液的试管中,观察到的现象是
A、B试管中无明显现象,C试管中铜丝表面有银白色物质析出
A、B试管中无明显现象,C试管中铜丝表面有银白色物质析出
,发生反应的化学方程式是Cu+2AgNO3→Cu(NO3)2+2Ag↓
Cu+2AgNO3→Cu(NO3)2+2Ag↓
.(2)用细线吊着的长玻璃棒的两端分别绕有40 cm长的铜丝(如右图所示),使玻璃棒保持平衡,用酒精
 灯加热玻璃棒左端2分钟后冷却,可以观察到的现象是
灯加热玻璃棒左端2分钟后冷却,可以观察到的现象是左端铜丝变成黑色,玻璃棒左端下沉
左端铜丝变成黑色,玻璃棒左端下沉
,产生该现象的原因是铜和空气中的氧气化合生成黑色的氧化铜,根据质量守恒定律氧化铜的质量大于参加反应的铜的质量
铜和空气中的氧气化合生成黑色的氧化铜,根据质量守恒定律氧化铜的质量大于参加反应的铜的质量
.(3)将四段相同长度的铜丝分别按下图所示放置一个月,观察并记录现象如下

F装置要研究的问题是
二氧化碳与铜生锈的反应是否有关
二氧化碳与铜生锈的反应是否有关
.结论:铜生锈是铜与
二氧化碳、水、氧气
二氧化碳、水、氧气
共同作用的结果.