网址:http://m.1010jiajiao.com/timu3_id_55903[举报]
甲同学设计以下实验制取氧气和氧化铜。
(1)制取氧气
①用20%的H2O2溶液,通过反应2H2O2MnO22H2O+O2↑来制取氧气,则在下列A、B、C三装置中最佳装置是______
 |
②与气体发生装置相连接的D装置的导管口是______
③为了能使产生的氧气被充分干燥,可采取的操作是
_________________________________________________________________________________
(2)制取氧化铜
将m g铜粉在氧气流中加热到高温,使铜粉全部氧化,得n g粉末X。乙同学查阅资料知:铜与氧气的反应有:①2Cu+O2△\s\up2 (——2CuO,②4CuO>1000℃2Cu2O+O2↑;在酸性条件下:2Cu+(aq)——Cu(s)+
Cu2+(aq)。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物并不一定是纯CuO,可能含有一定量的氧化亚铜(Cu2O)。
(3)探究铜的氧化物的成分
为测定粉末X中是否含有Cu2O,甲、乙、丙三同学分别设计如下实验方案。
甲同学的实验方案是:向粉末X加入稀硫酸,若有 ,则说明固体中含有Cu2O。
乙同学的实验方案是:再将粉末X放入氧气中加热,如果其质量增加,则说明其中含有Cu2O。
丙同学的实验方案是:通过分析实验数据就可以确定粉末X的成分。
若n的取值范围是 ≤n<_____,则粉末X中含有Cu2O,其物质的量是___________。
请你再设计一个与上述三个实验方案中现象不同的实验方案,通过对化学反应和对实验现象的分析来确定粉末X中是否含有Cu2O。写出该实验中离子反应的方程式。
查看习题详情和答案>>乙组:

丙组:

丁组:

戊组:

(1)甲组实验可用一个化学反应方程式表示为___________ ;使反应变快的可能原因是__________ ;从该反应器溶液(含有少量
 以抑制水解)中取得产品的实验操作步骤应为_________ 、_______ 、__________ ,取得产品后的残留物质可循环使用。
以抑制水解)中取得产品的实验操作步骤应为_________ 、_______ 、__________ ,取得产品后的残留物质可循环使用。 (2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染。则在五组方案中,__________ 组方案最好。
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
 ,便决定设计实验测定反应生成的
,便决定设计实验测定反应生成的 和O2的物质的量,并经计算确定该条件下
和O2的物质的量,并经计算确定该条件下 分解反应方程式中各物质的化学计量数。试验可能用到的仪器如下图所示:
分解反应方程式中各物质的化学计量数。试验可能用到的仪器如下图所示: 
① 准确称取6.0g无水;
②在试验结束时干燥管总质量增加2.4g;
③测得量筒中水的体积,得出气体在标准状况下的体积为280.mL;
试验结束时,装置F中的溶液只含NaHSO4和NaHSO3按装置从左到右的方向,各仪器接口连结顺序为: ①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(3)装置F的作用是__________。
(4)装置D的作用是__________。
(5)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温。 ②_____________ , ③________________ 。
(6)通过计算,推断出该条件下反应的化学方程式_______________________。
下图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示:

请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是_________________________。
(2)若按甲装置进行实验,则通入A的X是___________________,B中发生反应的化学方程式为______________________________。
(3)若按乙装置进行实验,则B管中应装入的物质是____________,B中发生反应的化学方程式为___________________________________________。
(4)两套装置中都需要加热的仪器有________(选填A、B、C)。
(5)请设计简单的实验,检验实验后C中所得液体确为甲醛溶液。简述所用试剂、操作、现象及结论。
_____________________________________________________________________
查看习题详情和答案>>已知:以铜作催化剂,用空气氧化醇制取醛,事实上是空气先与铜反应生成氧化铜,热的氧化铜再氧化醇生成醛。
某实验室中用甲醇、水、空气和铜粉(或氧化铜)制取甲醛溶液。下表给出甲醇、甲醛的沸点和水溶性:
图3-1是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示
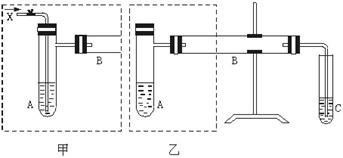
图3-1
请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是__________________________。
(2)若按甲装置进行实验,则通入A的X是______,B中发生反应的化学方程式为__________________________。
(3)若按乙装置进行实验,则B管中应装入的物质是______,B中发生反应的化学方程式为__________________________。
(4)试管C中应装入的试剂是__________。
(5)两套装置中都需要加热的仪器有______(填A、B、C)。
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?______(填“甲”或“乙”)。
(7)请设计简单的实验,检验实验后C中所得液体确为甲醛溶液。简述所用试剂、操作、现象及结论。
查看习题详情和答案>>已知:以铜作催化剂,用空气氧化醇制取醛,事实上是空气先与铜反应生成氧化铜,热的氧化铜再氧化醇生成醛。某实验室中用甲醇、水、空气和铜粉(或氧化铜)制取甲醛溶液。下表给出甲醇、甲醛的沸点和水溶性:
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 与水混溶 |
| 甲醛 | -21 | 与水混溶 |
下图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示
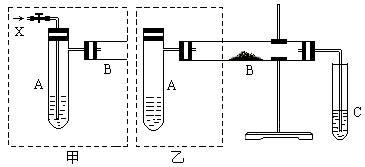
请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是____________________。
(2)若按甲装置进行实验,则通入A的X是______,B中发生反应的化学方程式为__________________________。(有机分子用结构式表示)
(3)若按乙装置进行实验,则B管中应装入的物质是__________。
(4)试管C中应装入的试剂是__________。
(5)两套装置中都需要加热的仪器有______(填A、B、C)。
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?______(填“甲”或“乙”)。
(7)验证实验后试管C中含有甲醛,所用试剂是__________。
查看习题详情和答案>>