网址:http://m.1010jiajiao.com/timu3_id_55235[举报]
(10分)A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。
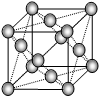
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中有 个σ键, ![]() 个π键。A6H6分子中A原子的杂化轨道类型是 杂化。
个π键。A6H6分子中A原子的杂化轨道类型是 杂化。
(2)当n =3时, A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是![]() (用元素符号表示),A、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(用元素符号表示),A、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(4)已知某红紫色络合物的组成为CoCl3?5NH3?H2O。该络合物中的中心离子钴离子在基态时核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
查看习题详情和答案>>(10分)A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中有 个σ键, 个π键。
(2)当n=3时, A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
 (4)已知某红紫色络合物的组成为CoCl3?5NH3?H2O。该络合物中的中心离子钴离子在基态时核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
(4)已知某红紫色络合物的组成为CoCl3?5NH3?H2O。该络合物中的中心离子钴离子在基态时核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
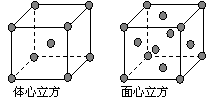
(5)金属铁的晶体在不同温度下有两种堆积方式, 晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 。
查看习题详情和答案>>
A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。
请回答下列问题:
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中
有 个σ键、 个π键。
(2)当n=3时,A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是 (用元素符号表示)。
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O。该配合物中的中心离子钴离子在基态时的核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
查看习题详情和答案>>A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。
请回答下列问题:
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中
有 个σ键、 个π键。
(2)当n=3时,A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是 (用元素符号表示)。
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O。该配合物中的中心离子钴离子在基态时的核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
查看习题详情和答案>>⑴当n=2时,AB2属于_______分子(填“极性”或“非极性”),分子中有_______个π键。A6H6分子中A原子的杂化轨道类型是_______杂化。
⑵当n=3时,A与B形成的晶体属于_______晶体。
⑶若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是_______(用元素符号表示)。
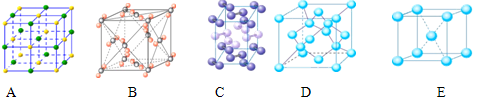
Ⅱ.⑴下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是__________(请用相应的编号填写)
⑶已知某红紫色配合物的组成为CoCl3·5NH3·H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为___________。
⑷下图是金属铝晶体结构的示意图。已知金属铝的密度为2.7g/cm3,则紧邻的铝原子的半径为_____________cm。(已知
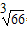 =4.04)
=4.04)