网址:http://m.1010jiajiao.com/timu3_id_55037[举报]
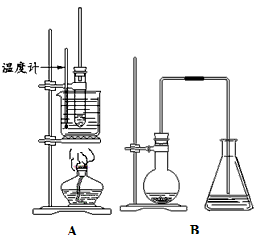
(1)基于相同的设计理念,两套装置有一个突出的共同点是________________________,这样设计的作用是________________________。
(2)实验室制取少量溴苯,应选用__________装置(填字母代号),写出该装置中发生的有机化学反应的化学方程式________________________。
(3)如果用制硝基苯的装置来制备少量一硝基甲苯(以甲苯为原料),实验中应该控制的反应温度与制备硝基苯相比应有什么不同之处________________________, 理由是________________________,写出一个制取一硝基甲苯的化学方程式________________________。
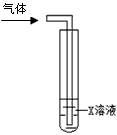
(4)用下图所示装置检验溴乙烷与NaOH的乙醇溶液共热产生的气体是否是乙烯。现有下列三种试剂: a. 溴水 b. Br2的CCl4溶液 c. KMnO4酸性溶液
如图所示,某同学设计了一个燃料电池并探究氯碱工业的原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题: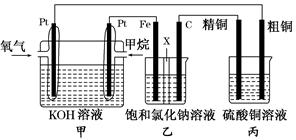
(1)甲烷燃料电池负极反应式为________________________。
(2)石墨(C)极的电极反应式为_______________________。
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成的气体的体积为________L;丙装置中阴极析出铜的质量为________ g。
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。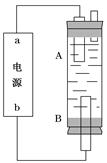
若用于制漂白液,a为电池的________极,电解质溶液最好用)________________
若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用________作电极。
(12分)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题: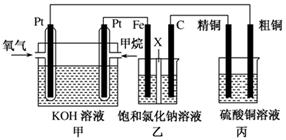
(1)甲烷燃料电池负极反应式是 ;
(2)石墨(C)极的电极反应式为 ;
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成 的气体体积为________L ,丙装置中阴极析出铜的质量为________g ;
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。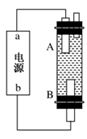
若用于制漂白液,a为电池的________极,电解质溶液最好用________;若用于制Fe(OH)2,使用硫酸钠作电解质溶液,阳极选用________作电极。

(1)甲烷燃料电池负极反应式是 ;
(2)石墨(C)极的电极反应式为 ;
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成 的气体体积为________L ,丙装置中阴极析出铜的质量为________g ;
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。

若用于制漂白液,a为电池的________极,电解质溶液最好用________;若用于制Fe(OH)2,使用硫酸钠作电解质溶液,阳极选用________作电极。
请回答下列问题:
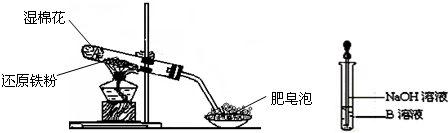
(1)硬质试管中发生反应的化学方程式为
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应.若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有