网址:http://m.1010jiajiao.com/timu3_id_55015[举报]
![]() (8分)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为: 2FeCl3+ Cu=2FeCl2+ CuCl2。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:www..com
(8分)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为: 2FeCl3+ Cu=2FeCl2+ CuCl2。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:www..com
①取少量废液,滴加KSCN溶液显红色。
②取10mL废液,加入足量的AgNO3溶液,析出沉淀8.6l g。
|
(1)根据有关数据计算该厂使用的FeCl3溶液中溶质的物质的量浓度 ▲ mol/L(假设腐蚀电路板后溶液体积不变)。
(2)试计算10mL废液中铜离子的物质的量是 ▲ mol。
选做题
选做题分为A、B两部分,请选择其中一部分作答。若两部分都做,则按B部分评分。www..com
A部分
查看习题详情和答案>>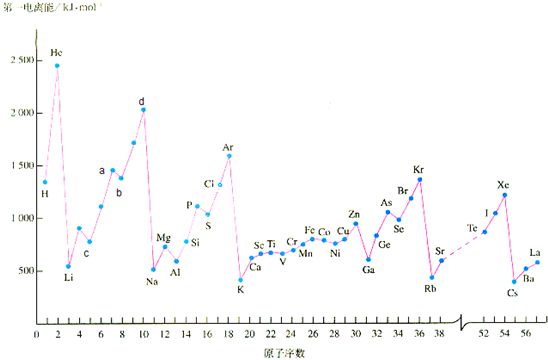
请回答下列问题:
(1)a点代表的元素是
(2)d点代表的元素的第一电离能处在峰顶原因是:
(3)上图中也给出了过渡元素的第一电离能数据,他们都与核外电子的排布有关,则Cu的外围电子排布式为:
(4)Mn 元素的外围电子排布式为3d54s2,Fe元素的外围电子排布式为3d64s2,请解释Mn的第三电离能比Fe的第三电离能大的原因是:
教材中给出了Na2O2与H2O反应的化学方程式。为了探究Na2O2与H2O反应的机理,某学习探究小组在教师指导下设计了如下图所示装置进行实验。

实验步骤如下:
①按图示组装仪器,并检查气密性为良好后装入药品;
②保持K1打开、K2关闭,将注射器中的水推入试管,此时A中无气体产生;
③挤压装有酚酞的胶头滴管,使酚酞滴入试管中,A中溶液显红色;
④挤压装有稀盐酸的胶头滴管,使稀盐酸滴入试管中,红色消失后再滴加2滴;
⑤用双连打气球向A中鼓气,使A中溶液通过喷头进入B中支管,发现淀粉KI溶液变蓝,KMnO4溶液褪色;
⑥迅速打开止水夹K2,关闭K1,继续向A中鼓气,待A中溶液进入C中约三分之一时停止鼓气。然后用热水浴加热C片刻,C中有气泡冒出,经检验为氧气。
回答下列问题:
(1) 写出Na2O2与H2O反应的离子方程式 ;
(2)若向Na2O2中滴加适量的盐酸,也能产生使带火星的木条复燃的气体,且最后溶液呈中性,请写出该反应的化学方程式 ;
(3)用离子方程式表示淀粉KI溶液变蓝的原因_____________________________ _;
(4)用离子方程式表示KMnO4溶液褪色的原因(MnO4-在酸性条件下被还原成Mn2+)
____________________________ ___ ;
(5)A中用冰盐冷浴和C中用热水浴的作用分别是________________________ ____,
;
(6)Na2O2与H2O反应的机理是(用化学方程式表示)______________________ ___,
。
查看习题详情和答案>>名称 | 分子式 | 颜色、状态 | 溶解性/g | 熔点/℃ | 密度/g·cm-3 |
乙二酸 | H2C2O4 | —— | 8.6(20℃) | 189.5 | 1.900 |
二水合乙二酸 | H2C2O4·2H2O | 无色晶体 | —— | 101.5 | 1.650 |
注:表中“——”表示尚未有具体数据。
回答下列问题:
(1)向盛有Na2CO3粉末的试管里加入约3 mL乙二酸溶液,观察到的现象为_____________;说明乙二酸的酸性比碳酸____________。
(2)向盛有5 mL乙二酸饱和溶液的试管中滴入3滴硫酸酸化的0.5%(质量分数)的KMnO4溶液,振荡,观察到现象为_______________________________________________________;说明乙二酸有______________________。
(3)向A试管中加入3 mL乙醇,然后,边振荡试管边加入2 mL 浓硫酸和2 mL乙二酸,按图甲连接好装置,加热3—5 min,在B试管中有油状、香味液体产生。该现象说明发生了______________(填有机反应类型)反应。在B试管中加入饱和Na2CO3溶液的目的是_______________________________________________________________。
导管在液面上的原因是________________________________________________。

(4)图乙是中学化学实验常用的装置,用此装置可制备的气体有___________(填标号)。
A.O2 B.H2 C.Cl2 D.NH3 E.CH2====CH2 F.CH![]() CH
CH
图乙试管口略低于试管底部的原因是_________________________________________。已知草酸分解的化学方程式为H2C2O4![]() H2O+CO2↑+CO↑。用图丙加热草酸晶体,验证草酸受热分解及其产物,图丙是中学化学教材中给出的实验装置图,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,指出图丙不合理的原因。
H2O+CO2↑+CO↑。用图丙加热草酸晶体,验证草酸受热分解及其产物,图丙是中学化学教材中给出的实验装置图,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,指出图丙不合理的原因。
答:______________________________________________________________。
该装置也不符合绿色化学的要求,因为________________________________________。
查看习题详情和答案>>

回答下列问题:
(1)向盛有Na2CO3粉末的试管里加入约3mL乙二酸溶液,观察到的现象为____; 说明乙二酸的酸性比碳酸____(填“强”或“弱”)。
(2)向盛有5mL乙二酸饱和溶液的试管中滴入3滴硫酸酸化的0.5%(质量分数)的KMnO4溶液,振荡,观察到的现象为__________ ;说明乙二酸有_________ 性。
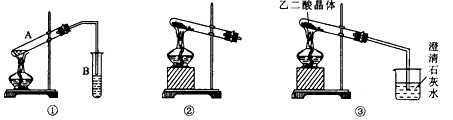
(3)向A试管中加入3mL乙醇,然后,边振荡试管边加入2mL浓硫酸和2mL乙二酸,按图①连接好装置,加 热3~5min,在B试管中有油状、香味液体产生。该现象说明发生了________ 反应(填有机反应类型)。在B试管中加入饱和Na2CO3溶液的目的是____;导管口在液面上方的目的是_____________ 。
A.O2
B.H2
C.Cl2
D.NH3
E.CH2=CH2
F.CH=CH
图②试管口要略低于试管底部的原因是_______________ 。
(5)已知草酸分解的化学方程式为H2C2O4
 H2O+CO2↑+CO↑。用图③加热草酸晶体,验证草酸受热分解及其产物,是原中学化学教材中给出的实验装置图,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,指出图③不合理的地方。 答:____________; 该装置也不符合绿色化学的要求,因为______________。
H2O+CO2↑+CO↑。用图③加热草酸晶体,验证草酸受热分解及其产物,是原中学化学教材中给出的实验装置图,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,指出图③不合理的地方。 答:____________; 该装置也不符合绿色化学的要求,因为______________。