摘要:27.已知椭圆中心在原点.抛物线的焦点为其右焦点.并且椭圆的长轴长.短轴 长.焦距成等差数列.A.B是椭圆上两点.弦AB的中点在直线x=4上. (1)求椭圆方程, (2)求证:弦AB的垂直平分线l与x轴交于定点.
网址:http://m.1010jiajiao.com/timu3_id_54088[举报]
实验室制CH4是用无水醋酸钠和碱石灰固体共热制取,其方程式为:H3COONa+NaOH![]() Na2CO3+CH4↑.回答:
Na2CO3+CH4↑.回答:
(1)实验室制取下列气体时,气体发生装置与实验室制取甲烷气体发生装置相同的是________.
①H2
②O2
③NH3
④NO
⑤Cl2
(2)现有如图所示的装置,可用它来收集CH4气体.收集时,配以不同的操作方法,会形成不同的收集方式.请简述CH4的三种收集方式.
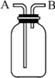
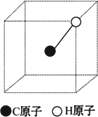
(3)已知CH4分子在空间呈四面体形状,1个C原子与4个H原子各共用一对电子形成4条共价键,C原子位于中心,4个H原子位于4个顶点.如图所示为一个立方体,已画出1个C原子(在立方体中心)、1个H原子(在立方体顶点)和1条共价键(实线表示),请画出另3个H原子的合适位置和3条共价键.
在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)?Ni(CO)4(g),已知该反应在25℃、80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
查看习题详情和答案>>
(2008?驻马店二模)某研究性学习小组的同学为在实验室再现二氧化硫催化氧化的过程,同时制取少量三氧化硫晶体,并测量反应后混合气体中SO2的含量,设计了如图所示的装置.

已知:V2O5在450℃左右,活性最好,温度过高或过低都会使催化剂活性下降.
(1)已知3.2g二氧化硫被氧气完全氧化成三氧化硫时,可以放出4.915kJ热量.则该反应的热化学方程式为
(2)A装置可用来观察SO2和氧气的进气量.实验时使A中氧气导管冒出的气泡与SO2导管冒出的气泡速率相近,其目的是
(3)检查完装置的气密性且加入药品后,开始进行实验.此时首先应该进行的操作是
(4)在实验过程中不能持续加热的理由是
(5)冰盐水的作用是
(6)能用于测定反应后混合气体中SO2含量的是
A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液 D.氨水、酚酞试液.
查看习题详情和答案>>

已知:V2O5在450℃左右,活性最好,温度过高或过低都会使催化剂活性下降.
(1)已知3.2g二氧化硫被氧气完全氧化成三氧化硫时,可以放出4.915kJ热量.则该反应的热化学方程式为
2SO2(g)+O2(g)?2SO3(g),△H=-196.6kJ/mol
2SO2(g)+O2(g)?2SO3(g),△H=-196.6kJ/mol
.(2)A装置可用来观察SO2和氧气的进气量.实验时使A中氧气导管冒出的气泡与SO2导管冒出的气泡速率相近,其目的是
使用过量氧气以提高SO2的转化率
使用过量氧气以提高SO2的转化率
.(3)检查完装置的气密性且加入药品后,开始进行实验.此时首先应该进行的操作是
加热(或点燃酒精灯)
加热(或点燃酒精灯)
.(4)在实验过程中不能持续加热的理由是
该反应为放热反应,温度过高催化剂活性降低
该反应为放热反应,温度过高催化剂活性降低
.(5)冰盐水的作用是
降温,冷却SO3使之成为晶体
降温,冷却SO3使之成为晶体
.(6)能用于测定反应后混合气体中SO2含量的是
BC
BC
(填字母)A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液 D.氨水、酚酞试液.
已知FeC2O4?2H2O 在受热先失去结晶水,继续加热FeC2O4分解为气体和一种铁的氧化物,某实验小组利用如下装置(部分固定和加热装置略)探究草酸钙分解气体部分产物及固体产物的实验式.
(1)请指出该装置一处缺陷:
(2)完善并连好装置后,需进行的实验操作有:① ;②加药品和试剂;③给A、C装置加热…
(3)若分解的气体中含有CO,则观察到的现象是 .
(4)甲同学欲要检测得到的固体是否含有+3价的铁元素,他应该选择的试剂是 (填序号)
A.KSCN溶液 B.稀硝酸 C.稀硫酸 D.铁粉
(5)若实验前将3.6g草酸亚铁晶体(FeC2O4?2H2O)加入大试管加热分解,充分反应后得到1.44g黑色固体,则该铁的氧化物是 .(填化学式)
查看习题详情和答案>>

(1)请指出该装置一处缺陷:
(2)完善并连好装置后,需进行的实验操作有:①
(3)若分解的气体中含有CO,则观察到的现象是
(4)甲同学欲要检测得到的固体是否含有+3价的铁元素,他应该选择的试剂是
A.KSCN溶液 B.稀硝酸 C.稀硫酸 D.铁粉
(5)若实验前将3.6g草酸亚铁晶体(FeC2O4?2H2O)加入大试管加热分解,充分反应后得到1.44g黑色固体,则该铁的氧化物是
已知某盐在不同温度下的溶解度如右表.若把质量百分比浓度为22%的该盐溶液由50℃逐渐冷却,则开始析出晶体的温度范围是( )
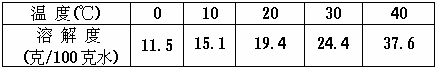

| A、0~10℃ | B、10~20℃ | C、20~30℃ | D、30~40℃ |