摘要:实验设计内容 概括地讲.设计一个实验通常包括以下几个方面内容: (1)根据命题要求.说明设计该实验的原理.画出实验装置. (2)列出实验操作步骤.说明实验中应注意的事项. (3)观察.记录实验现象.分析实验结果(包括写出有关的化学方程式).得出正确的结论.
网址:http://m.1010jiajiao.com/timu3_id_52344[举报]
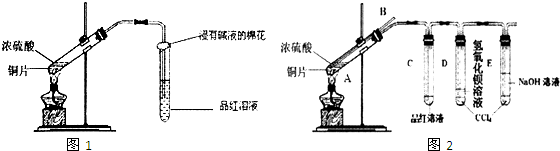
某研究性学习小组为探究Cu与浓H2SO4的反应及其产物SO2的性质,设计如图1实验装置:
(1)写出铜与浓硫酸反应的化学方程式: ;浸有碱液的棉花的作用是 .
(2)该小组同学在实验中发现以上实验装置有相当多不足之处,如实验不够安全和易造成环境污染等.为改进实验和更多地了解SO2的性质,经过同学问的讨论和与老师的交流,设计了如图2实验装置.
①请写出长导管B的作用 (只写一点就可).
②对试管A中的浓H2SO4和铜片进行加热,发现E试管中有气泡逸出,品红溶液很快褪色,但最终未见D试管中氢氧化钡溶液出现浑浊.为探究D试管中未出现浑浊的原因,该小组同学在化学手册中只查阅到下列物质常温下的溶解度数据:
请你应用类比研究方法帮他们预测D试管未出现浑浊的原因: .
③为验证D试管中溶液的组成,进行了下列实验,请你帮他们完成下列实验内容:
 查看习题详情和答案>>
查看习题详情和答案>>
(1)写出铜与浓硫酸反应的化学方程式:
(2)该小组同学在实验中发现以上实验装置有相当多不足之处,如实验不够安全和易造成环境污染等.为改进实验和更多地了解SO2的性质,经过同学问的讨论和与老师的交流,设计了如图2实验装置.
①请写出长导管B的作用
②对试管A中的浓H2SO4和铜片进行加热,发现E试管中有气泡逸出,品红溶液很快褪色,但最终未见D试管中氢氧化钡溶液出现浑浊.为探究D试管中未出现浑浊的原因,该小组同学在化学手册中只查阅到下列物质常温下的溶解度数据:
| 物质 | 溶解度(g/100水) | 物质 | 溶解度(g/100水) |
| Ca(OH)2 | 0.173 | Ba(OH)2 | 3.89 |
| CaCO3 | 0.0013 | BaSO3 | 0.016 |
| Ca(HCO3)2 | 16.60 |
③为验证D试管中溶液的组成,进行了下列实验,请你帮他们完成下列实验内容:
| 实验方案 | 现象 |
| 1.取少量溶液于试管中,加入稀盐酸,加热, 用湿润的蓝色石蕊试纸检验生成的气体. |
|
| 2.取少量溶液于试管中,加入 |
 查看习题详情和答案>>
查看习题详情和答案>>
为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,实验设计和实验过程如下:
如图连接好装置,向烧杯中加入25 mL 1 mol/L的Ba(OH)2溶液和2滴酚酞试剂,再一边不断地滴加1 mol/L的H2SO4溶液,并轻轻振荡。试完成下列内容:
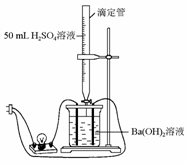
(1)实验现象及分析:①溶液颜色变化为__________,
原因____________________________________。
②灯泡亮度变化:____________________________,
原因____________________________________。
③溶液变浑浊,原因________________________________________________。
(2)实验结论:稀H2SO4与Ba(OH)2溶液反应的实质是______________________(可用离子方程式解释)。
查看习题详情和答案>>
某校化学兴趣小组在探究铁与浓硫酸的反应时,将教材中铜与浓硫酸反应的实验装置(图Ⅰ)改为图Ⅱ所示的装置.
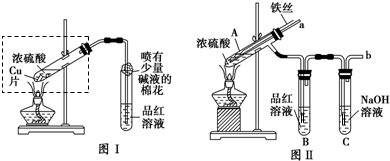
请回答下列问题:
(1)写出图Ⅰ中虚框处发生反应的化学方程式 .
(2)图Ⅱ实验装置与图Ⅰ相比较,其优点是:①能更好地吸收有毒气体SO2,防止其污染环境;② .
(3)下列对导管a的作用分析中正确的是 (填字母).
A.加热反应过程中,可上下移动导管a,起搅拌作用
B.停止加热,试管内的压强减小,从导管a进入的空气可增大试管A内的压强,防止倒吸
C.停止反应,撤装置之前往导管a中通入空气,可排除装置内的SO2气体,防止其污染环境
(4)反应一段时间后,将试管A取下,然后将试管A中溶液倒入另一盛有适量水的试管D中.该小组同学为确定溶液中所存在的金属离子,进行下列探究过程.
①提出假设:
假设Ⅰ:只含有Fe3+.假设Ⅱ: .假设Ⅲ: .
②实验设计:
分别取少量试管D中溶液,选用提供的试剂,设计简单的实验检验溶液中所存在的金属离子.请填写下表空白(可以不填满,也可以增加).
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液.
查看习题详情和答案>>

请回答下列问题:
(1)写出图Ⅰ中虚框处发生反应的化学方程式
(2)图Ⅱ实验装置与图Ⅰ相比较,其优点是:①能更好地吸收有毒气体SO2,防止其污染环境;②
(3)下列对导管a的作用分析中正确的是
A.加热反应过程中,可上下移动导管a,起搅拌作用
B.停止加热,试管内的压强减小,从导管a进入的空气可增大试管A内的压强,防止倒吸
C.停止反应,撤装置之前往导管a中通入空气,可排除装置内的SO2气体,防止其污染环境
(4)反应一段时间后,将试管A取下,然后将试管A中溶液倒入另一盛有适量水的试管D中.该小组同学为确定溶液中所存在的金属离子,进行下列探究过程.
①提出假设:
假设Ⅰ:只含有Fe3+.假设Ⅱ:
②实验设计:
分别取少量试管D中溶液,选用提供的试剂,设计简单的实验检验溶液中所存在的金属离子.请填写下表空白(可以不填满,也可以增加).
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液.
| 步骤 | 所选试剂 | 现象及结论 |
| 1 | ||
| 2 | ||
| 3 |
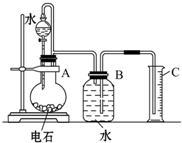 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.(1)烧瓶中发生反应的化学方程式为
CaC2+2H2O→Ca(OH)2+C2H2↑
CaC2+2H2O→Ca(OH)2+C2H2↑
.装置B、C的作用是装置B用于贮水以便烧瓶中生成的C2H2气体进入B时排出与它等体积的水进入量筒C来测定生成乙炔的量;
装置B用于贮水以便烧瓶中生成的C2H2气体进入B时排出与它等体积的水进入量筒C来测定生成乙炔的量;
.(2)分液漏斗与烧瓶间用乳胶管连接的目的是
便于液体顺利滴下
便于液体顺利滴下
.(3)所用电石质量不能太大,否则
生成C2H2太多超过B的空间
生成C2H2太多超过B的空间
;也不能太小,否则无法测定其体积测定误差会更大
无法测定其体积测定误差会更大
;若容器B的容积为250mL,则所用电石的质量应在0.60
0.60
g左右(从后面数据中选填:0.03、0.60、1.00、1.50、2.00).(4)为了得到比较平稳的乙炔气流,实验室通常用
饱和食盐水
饱和食盐水
代替水进行实验.(5)实验中测得排入量筒中水的体积为VL、电石的质量为Wg.则电石中碳化钙的质量分数是
| 0.29V |
| W |
| 0.29V |
| W |
全世界每年因生锈损失的钢铁约占世界钢铁年产量的
.某学生想探究铁生锈的条件,他将干净的铁钉分别同时入放A、B、C三支试管中进行研究.
(1)请你帮助该学生完成下列实验设计的内容:
(2)一周后,编号为
(3)用相同材料制作,经过相同时间防锈处理的铁栏杆,安装在南方比安装在北方更易生锈,其原因是
查看习题详情和答案>>
| 1 |
| 4 |
(1)请你帮助该学生完成下列实验设计的内容:
| 编号 | 操作方法 | 实验目的 |
| A | 向干燥试管A中放入干燥的铁钉,并用橡皮塞塞上 向干燥试管A中放入干燥的铁钉,并用橡皮塞塞上 |
探究铁在干燥空气中的生锈情况 |
| B | 放入铁钉,注入蒸馏水浸没铁钉,并用植物油液封 | 探究铁钉在水中的生锈情况 探究铁钉在水中的生锈情况 |
| C | 将铁钉放入试管C中,加入蒸馏水浸没铁钉一半,敞口放置 将铁钉放入试管C中,加入蒸馏水浸没铁钉一半,敞口放置 |
探究铁在有空气和水封时的生锈情况 |
C
C
的试管中的铁钉最易生锈.证明铁生锈的条件的条件是在有水和氧气时铁最易生锈
在有水和氧气时铁最易生锈
.(3)用相同材料制作,经过相同时间防锈处理的铁栏杆,安装在南方比安装在北方更易生锈,其原因是
南方雨水多,空气中水汽含量高,所以铁更容易生锈
南方雨水多,空气中水汽含量高,所以铁更容易生锈
.