网址:http://m.1010jiajiao.com/timu3_id_52228[举报]
已知氯化铁溶液能与碘化钾反应生成氯化亚铁、氯化钾和碘单质。某溶液中含有的溶质是FeBr2、FeI2,若向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变成血红色,则下列叙述正确的是( )
①原溶液中的Br―一定被氧化
②通入氯气后原溶液中的Fe2+一定被氧化;
③不能确定通入氯气之后的溶液中是否存在Fe2+;
④若取少量所得溶液,再加入CCl4,静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的Fe2+、Br―、I―均被完全氧化
A.只有②③ B.只有②③④ C.只有①④ D.①②③④
查看习题详情和答案>>Ⅰ.溴水和氯化铁溶液是中学化学实验中的常用试剂,浓度较小时,溶液均呈黄色。某同学将稀溴水和稀FeCl2溶液混合,所得溶液显黄色。为探究溴水和FeCl2溶液混合能否发生反应,该同学设计了以下实验方案:
| 操作 | 实验现象 | 实验结论 | |
| 方案1 | 取少量混合溶液,加入NaOH溶液,振荡 | 得到红褐色沉淀 | 发生了化学反应 |
| 方案2 | 取少量混合溶液,加入四氯化碳溶液,振荡 | 有机层呈橙黄色 | 未发生化学反应 |
| 方案3 | 取少量混合溶液,加入淀粉碘化钾溶液,振荡 | 溶液变蓝色 | 未发生化学反应 |
请回答下列问题:
(1)方案2的结论不合理,其理由是
(2)方案3的结论明显不合理,可能发生反应的离子方程式
(3)请另外设计一个简单的实验方案(包括“操作”“现象”“结论”),判断溴水和FeCl2溶液是否反应。
。
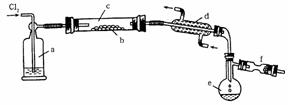 Ⅱ.S2Cl2是一种易挥发的液体(熔点:-76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
Ⅱ.S2Cl2是一种易挥发的液体(熔点:-76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
(1)装置a中应放试剂为__________;装置d的名称是_________,它的作用是_________。
(2)该实验的操作顺序应为__________(用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(3)将S2Cl2的水解气体产物通入氯水中,若观察到_________的现象,则可证明水解产物中有硫化氢生成。
查看习题详情和答案>>A.Al2S3和Fe2S3 B.Fe(OH)3和Al(OH)3
C.FeS、Al(OH)3和I2 D.FeS、Al(OH)3和S 查看习题详情和答案>>
(1)向其中投入少量金属钠,现象是___,反应的化学方程式是____。
(2)向其中加入过量铁粉,现象是 ____,反应的化学方程式是 ____。将反应后的溶液分装在两支试管中,一支试管中加入氯水,现象是 ____,反应的离子方程式是____ 。另一支试管中加入氢氧化钠溶液,现象是 ____,反应的化学方程式是____。
(3)向其中加入足量的碘化钾淀粉溶液,溶液的颜色呈蓝色,其反应的离子方程式为____ 。
(4)向其中通入硫化氢气体,现象是___ ,反应的离子方程式是___ ,溶液的酸性___。
(5)给FeCl3溶液小心加热至出现红褐色,反应的化学方程式为____。
(1)在其水溶液中投入少量金属钠,现象是_______________________________,反应方程式为_____________________________。
(2)在其水溶液中加入过量铁粉,现象是_________________________________,反应方程式为_____________________。将变化后的溶液分装两个试管,一个试管中加入氯水,现象是_______________________,反应方程式为__________________________________;另一试管中加入NaOH溶液,现象是______________________________________,反应方程式为__________________________________。
(3)在其水溶液中加入足量的碘化钾淀粉溶液,溶液的颜色呈________色,其反应方程式为____________________________________________。
(4)如配制0.1 mol·L-1的FeCl3溶液500 mL,需FeCl3·6H2O________g。
查看习题详情和答案>>