摘要:18.[数据处理] 解:生成H2的质量:102.4g+247.3g-348.7g=1.0g 设生铁样品中含铁的质量为x. Fe+H2SO4 == FeSO4+H2↑ 56 2 x 1.0g 生铁样品中铁单质的质量分数为 %=87.5% 答:生铁样品中铁单质的质量分数是87.5%. [交流讨论] ⑴左 ⑵确保生铁样品中铁单质与稀硫酸完全反应 ⑶8.25%
网址:http://m.1010jiajiao.com/timu3_id_5210[举报]
牙膏(如图1)是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分.

提出问题1:某品牌牙膏中是否含有CaCO3?
查阅资料:二氧化硅不与稀盐酸反应
实验方案:
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有
②取实验①中的溶液,加入草酸铵[(NH4)2C2O4]溶液,生成白色沉淀--草酸钙,请写出该反应的化学方程式
提出问题2:该牙膏中CaCO3的含量是多少?
实验装置:如图2
实验步骤:
(1)按如图2连接好装置后,发现一处明显的错误,改正为
(2)重新连接好装置,并
(3)在B装置中加入牙膏样品8.00g;
(4)
(5)
(6)将C装置中的固液混合物过滤、
(7)重复实验.
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)
实验数据:重复实验,3次数据记录如下:
实验分析及数据处理:
(1)上述数据能否由托盘天平测得?
(2)若没有A装置,则测定结果将
(3)D装置的作用是
(4)据上表数据,计算该牙膏样品中CaCO3的含量是多少?
写出计算过程
实验反思:
(1)重复实验,取平均值的意义在于
(2)下列各项措施中,能提高测定准确度的是
a.在装置A、B之间增加盛有浓硫酸的洗气瓶
b.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c.缓缓滴加稀盐酸.
查看习题详情和答案>>

提出问题1:某品牌牙膏中是否含有CaCO3?
查阅资料:二氧化硅不与稀盐酸反应
实验方案:
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有
CO32-
CO32-
离子;②取实验①中的溶液,加入草酸铵[(NH4)2C2O4]溶液,生成白色沉淀--草酸钙,请写出该反应的化学方程式
(NH4)2C2O4+CaCl2=2NH4Cl+CaC2O4↓
(NH4)2C2O4+CaCl2=2NH4Cl+CaC2O4↓
.提出问题2:该牙膏中CaCO3的含量是多少?
实验装置:如图2
实验步骤:
(1)按如图2连接好装置后,发现一处明显的错误,改正为
C中导管应“长进短出”
C中导管应“长进短出”
;(2)重新连接好装置,并
检查装置的气密性
检查装置的气密性
;(3)在B装置中加入牙膏样品8.00g;
(4)
关闭
关闭
K1,打开
打开
K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至B中不再产生气泡
B中不再产生气泡
,停止滴加盐酸;(5)
关闭K2,打开K1,缓缓通入空气
关闭K2,打开K1,缓缓通入空气
,至C中不再产生沉淀;(6)将C装置中的固液混合物过滤、
洗涤
洗涤
、烘干后称量其质量;(7)重复实验.
(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)
实验数据:重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| D装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)上述数据能否由托盘天平测得?
不能
不能
.(2)若没有A装置,则测定结果将
偏大
偏大
.(填“偏大”、“偏小”或“不变”)(3)D装置的作用是
吸收空气中的二氧化碳干扰,防止干扰实验测定
吸收空气中的二氧化碳干扰,防止干扰实验测定
.(4)据上表数据,计算该牙膏样品中CaCO3的含量是多少?
写出计算过程
解:根据三次数据求得生成沉淀的平均值为3.94g,设参加反应的二氧化碳的质量为x
Ba(OH)2+CO2═BaCO3↓+H2O
44 197
x 3.94g
=
x=0.88g
设碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
y0.88g
=
y=2.00g
答:该牙膏样品中碳酸钙的质量是2.00g.
Ba(OH)2+CO2═BaCO3↓+H2O
44 197
x 3.94g
| 44 |
| x |
| 197 |
| 3.94g |
x=0.88g
设碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
y0.88g
| 100 |
| y |
| 44 |
| 0.88g |
y=2.00g
答:该牙膏样品中碳酸钙的质量是2.00g.
解:根据三次数据求得生成沉淀的平均值为3.94g,设参加反应的二氧化碳的质量为x
Ba(OH)2+CO2═BaCO3↓+H2O
44 197
x 3.94g
=
x=0.88g
设碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
y0.88g
=
y=2.00g
答:该牙膏样品中碳酸钙的质量是2.00g.
.Ba(OH)2+CO2═BaCO3↓+H2O
44 197
x 3.94g
| 44 |
| x |
| 197 |
| 3.94g |
x=0.88g
设碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
y0.88g
| 100 |
| y |
| 44 |
| 0.88g |
y=2.00g
答:该牙膏样品中碳酸钙的质量是2.00g.
实验反思:
(1)重复实验,取平均值的意义在于
减小偶然误差(合理即可)
减小偶然误差(合理即可)
.(2)下列各项措施中,能提高测定准确度的是
bc
bc
(填序号).a.在装置A、B之间增加盛有浓硫酸的洗气瓶
b.在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c.缓缓滴加稀盐酸.
 小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验:
小璐和小磊合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计进行了如下两个探究实验:[实验1]取20g该混合酸并分成4等份,分别加入一定量未知质量分数的BaCl2溶液,记录如下:
| 第1份 | 第2份 | 第3份 | 第4份 | |
| 加入BaCl2溶液的质量/g | 15 | 20 | 25 | 30 |
| 反应得到的沉淀的质量/g | 1.398 | 1.864 | 2.330 | 2.330 |
[数据处理]
小璐依据[实验1]沉淀的质量计算出混合酸中H2SO4的质量分数.
小磊依据[实验2]求混合酸中HCl的质量分数,过程如下:
解:设混合酸中HCl的质量分数为ω.
HCl+NaOH=NaCl+H2O
36.5 40
| 20g |
| 4 |
解得:ω=0.1825=18.25%
现请你参与探究并完成相关问题.
(1)[实验1]中发生反应的化学方程式为
BaCl2+H2SO4=2HCl+BaSO4↓.
BaCl2+H2SO4=2HCl+BaSO4↓.
.(2)根据小璐的计算,测出原混合酸中H2SO4的质量分数为多少?(保留三位有效数字).
[反思交流]小磊计算出混合酸中HCl的质量分数会
偏高
偏高
(填“偏高”、“偏低”或“无影响”),理由是因为BaCl2与H2SO4反应后有盐酸生成,从而使滤液中的盐酸的质量增大.
因为BaCl2与H2SO4反应后有盐酸生成,从而使滤液中的盐酸的质量增大.
(如“无影响”,本空不作答).
草酸亚铁晶体(化学组成为FeC2O4?xH2O)是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
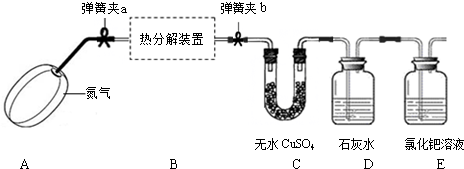
【实验步骤】:
①连接好装置,
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(提示:相对分子质量分别为FeC2O4:144; H2O:18)
(5)实验过程中,鼓入氮气的目的是
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁.你认为这种说法是否正确?请说出可能的理由
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么?
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式
查看习题详情和答案>>

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):

【实验步骤】:
①连接好装置,
检查气密性
检查气密性
;②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④
关闭弹簧夹a
关闭弹簧夹a
,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
| 装置B的质量(/g) | 装置C的质量(/g) | |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g | ||
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了
水
水
,FeC2O4?xH2O中x的值为2
2
;(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了
CO
CO
;(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了
CO2
CO2
;(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(提示:相对分子质量分别为FeC2O4:144; H2O:18)
FeO
FeO
;(5)实验过程中,鼓入氮气的目的是
排尽装置中的空气,以免黑色的残留物(或FeO)被氧化
排尽装置中的空气,以免黑色的残留物(或FeO)被氧化
;(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式
FeC2O4?2H2O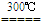 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O
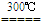 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2OFeC2O4?2H2O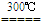 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O
;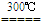 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁.你认为这种说法是否正确?请说出可能的理由
不正确,因为温度达不到工业炼铁所需的高温,所以不能相互反应生成Fe
不正确,因为温度达不到工业炼铁所需的高温,所以不能相互反应生成Fe
;(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么?
没有尾气处理装置,会造成CO污染空气;
没有尾气处理装置,会造成CO污染空气;
;(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式
4FeO+O2═2Fe2O3
4FeO+O2═2Fe2O3
.甲、乙两位同学在学习甲烷性质时,发现甲烷与氢气和一氧化碳性质上有很多相似之处,如密度比空气小,难溶于水,具有可燃性等.但H2和CO具有还原性,那么甲烷有没有还原性呢?
【假设猜想】甲同学:甲烷没有还原性
乙同学:甲烷有还原性,并对甲烷还原氧化铜的产物提出了下列假设:
假设1:Cu、CO2
假设2:Cu、CO、H2O
假设3:Cu、CO2、H2O
假设4:Cu、CO、CO2、H2O
其中假设
【查阅资料】无水硫酸铜遇水由白色变为蓝色
【设计实验步骤】(假设药品都是足量的)为了判断假设的合理性,乙同学设计了以下装置
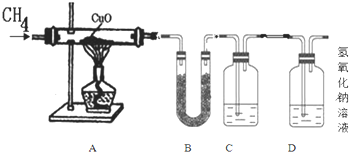
①分别称量装置A、B、C的质量
②再次分别称量装置A、B、C的质量
③向玻璃管中装入CuO通一段时间的CH4
④停止加热,继续通入CH4至冷却到室温
⑤缓缓通入足量的CH4,加热装置A,使其充分反应
甲同学认为还缺少一个步骤,缺少的步骤是⑥
【进行实验】乙同学按照正确的步骤进行实验,并记录了实验现象和数据
①装置A中的黑色粉末变红;装置B中白色粉末变蓝;装置C中石灰水变浑浊
②称量数据如表所示.
【现象分析与数据处理】
根据装置A、B、C中的现象可推知,CH4与CuO充分反应后的产物依次是
【实验结论】
①CH4
②装置A中发生的反应方程式为
查看习题详情和答案>>
【假设猜想】甲同学:甲烷没有还原性
乙同学:甲烷有还原性,并对甲烷还原氧化铜的产物提出了下列假设:
假设1:Cu、CO2
假设2:Cu、CO、H2O
假设3:Cu、CO2、H2O
假设4:Cu、CO、CO2、H2O
其中假设
1
1
不合理,理由是甲烷中含有氢元素
甲烷中含有氢元素
【查阅资料】无水硫酸铜遇水由白色变为蓝色
【设计实验步骤】(假设药品都是足量的)为了判断假设的合理性,乙同学设计了以下装置

①分别称量装置A、B、C的质量
②再次分别称量装置A、B、C的质量
③向玻璃管中装入CuO通一段时间的CH4
④停止加热,继续通入CH4至冷却到室温
⑤缓缓通入足量的CH4,加热装置A,使其充分反应
甲同学认为还缺少一个步骤,缺少的步骤是⑥
检查装置的气密性
检查装置的气密性
,其合理的操作顺序是⑥①③⑤④②
⑥①③⑤④②
(填序号).【进行实验】乙同学按照正确的步骤进行实验,并记录了实验现象和数据
①装置A中的黑色粉末变红;装置B中白色粉末变蓝;装置C中石灰水变浑浊
②称量数据如表所示.
| A中玻璃管(含药品)质量 | 装置B的质量 | 装置C的质量 | |
| 反应前 | 150g | 156.6g | 256.8g |
| 反应后 | 147.2g | 158.4g | 257.9g |
根据装置A、B、C中的现象可推知,CH4与CuO充分反应后的产物依次是
Cu H2OCO2
Cu H2OCO2
.【实验结论】
①CH4
有
有
(填“有”或“没有”)还原性.如没有,不作答;如有,则乙同学的假设4
4
正确,原因是根据质量守恒定律,生成的二氧化碳中碳元素的质量为0.3g,生成的水中氢元素的质量为0.2g,C:H=3:2而甲烷中C:H=4:1,因此还生成CO.
根据质量守恒定律,生成的二氧化碳中碳元素的质量为0.3g,生成的水中氢元素的质量为0.2g,C:H=3:2而甲烷中C:H=4:1,因此还生成CO.
②装置A中发生的反应方程式为
2CH4+7CuO
7Cu+4H2O+CO+CO2
| ||
2CH4+7CuO
7Cu+4H2O+CO+CO2
.
| ||
(2012?扬中市模拟)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献.他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O═NH4HCO3;
NH4HCO3+NaCl═NaHCO3↓+NH4Cl;
2NaHCO3
Na2CO3+CO2↑+H2O
回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解 c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).
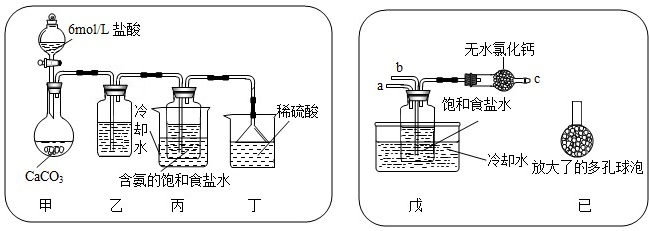
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 饱和的碳酸氢钠溶液,作用是
(Ⅱ)丁装置中稀硫酸的作用是
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是
②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:
(4)“纯碱中常常会混有少量氯化钠.”某研究性学习小组以一包纯碱(只考虑含氯化钠)为研究对象,探究纯碱样品中碳酸钠的含量.
【实验设计】
甲方案
Ⅰ.设计思路:根据样品与氯化钙溶液反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ.操作步骤:称取13.25g纯碱样品,加入过量的氯化钙溶液,充分搅拌.过滤、洗涤、干燥,得到的白色沉淀10.00g.
Ⅲ.数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
乙方案
I.设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
II.实验结论:
(1)当a、b的质量关系满足
=
(或22a=53b;或a=
b等)
=
(或22a=53b;或a=
b等)(填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100%.
(2)当a、b的质量关系满足
>
>
时,纯碱样品室有碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是
×100%
×100%.
【实验评价】
误差分析:
(一)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.如果将氯化钙溶液换成氯化钡溶液,则可以使误差减小,理由是
(二)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比
查看习题详情和答案>>
NH3+CO2+H2O═NH4HCO3;
NH4HCO3+NaCl═NaHCO3↓+NH4Cl;
2NaHCO3
| ||
回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是
c
c
(填字母标号).a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解 c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).

试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 饱和的碳酸氢钠溶液,作用是
吸收甲装置可能挥发出的氯化氢气体
吸收甲装置可能挥发出的氯化氢气体
;(Ⅱ)丁装置中稀硫酸的作用是
吸收末反应的NH3
吸收末反应的NH3
;(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是
过滤
过滤
(填分离操作的名称).②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从
a
a
管通入氨气
氨气
气体;(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是
增大气体与溶液接触面积,提高CO2吸收率
增大气体与溶液接触面积,提高CO2吸收率
;(3)请你再写出一种实验室制取少量碳酸氢钠的方法:
用碳酸氢铵与适量饱和食盐水反应.(或往烧碱溶液中通入过量CO2;往饱和Na2CO3 溶液中通入过量CO2 等.其他合理方法均可)
用碳酸氢铵与适量饱和食盐水反应.(或往烧碱溶液中通入过量CO2;往饱和Na2CO3 溶液中通入过量CO2 等.其他合理方法均可)
.(4)“纯碱中常常会混有少量氯化钠.”某研究性学习小组以一包纯碱(只考虑含氯化钠)为研究对象,探究纯碱样品中碳酸钠的含量.
【实验设计】
甲方案
Ⅰ.设计思路:根据样品与氯化钙溶液反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
Ⅱ.操作步骤:称取13.25g纯碱样品,加入过量的氯化钙溶液,充分搅拌.过滤、洗涤、干燥,得到的白色沉淀10.00g.
Ⅲ.数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数.
计算过程:
解:设纯碱样品中含Na2CO3的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.00g
=
x=10.6g
纯碱样品中Na2CO3的质量分数为
×100%=80%
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.00g
| 106 |
| 100 |
| x |
| 10.00g |
x=10.6g
纯碱样品中Na2CO3的质量分数为
| 10.6g |
| 13.25g |
解:设纯碱样品中含Na2CO3的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.00g
=
x=10.6g
纯碱样品中Na2CO3的质量分数为
×100%=80%
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.00g
| 106 |
| 100 |
| x |
| 10.00g |
x=10.6g
纯碱样品中Na2CO3的质量分数为
| 10.6g |
| 13.25g |
乙方案
I.设计思路:根据样品(质量为a g)与稀硫酸完全反应生成二氧化碳的质量(质量为b g),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数.
II.实验结论:
(1)当a、b的质量关系满足
| a |
| b |
| 53 |
| 22 |
| 53 |
| 22 |
| a |
| b |
| 53 |
| 22 |
| 53 |
| 22 |
(2)当a、b的质量关系满足
| a |
| b |
| 53 |
| 22 |
| a |
| b |
| 53 |
| 22 |
| 53b |
| 22a |
| 53b |
| 22a |
【实验评价】
误差分析:
(一)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小.如果将氯化钙溶液换成氯化钡溶液,则可以使误差减小,理由是
BaCl2比CaCl2的相对分子质量大,产生的沉淀质量大,称量误差小
BaCl2比CaCl2的相对分子质量大,产生的沉淀质量大,称量误差小
.(二)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比
偏小
偏小
(填“偏大”、“偏小”、或“不变”).