摘要:用NaOH.H2O.大理石和盐酸制取33 g纯NaHCO3.请参照物质的溶解度回答下列问题: 25℃ 溶解度/g NaOH 100 NaHCO3 9 Na2CO3 30 (1)写出制取过程中反应的化学方程式. (2)若提供100 g水.则需NaOH的物质的量为多少? (3)简述实验的操作过程. (4)在上图反映上述实验过程的图象中.标出A点[即当n(CO2)/n=1/3.且n(CO2)=0.125 mol]的位置.并判断此时所得盐的组成及其物质的量.
网址:http://m.1010jiajiao.com/timu3_id_51598[举报]
电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料.工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了提取流程图1:
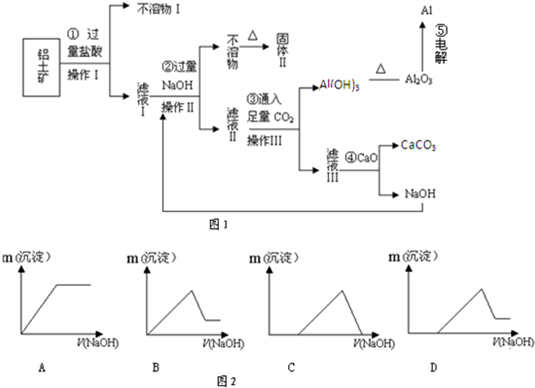
(1)固体Ⅱ的化学式为_
(2)写出流程③的离子方程式
(3)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应
(4)从铝土矿中提取铝的过程不涉及的化学反应类型是
A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(5)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有
(6)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系(图2)中正确的是
查看习题详情和答案>>

(1)固体Ⅱ的化学式为_
Fe2O3
Fe2O3
,该固体的颜色为红棕色
红棕色
;(2)写出流程③的离子方程式
AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-
AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-
;(3)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应
放出大量的热
放出大量的热
;(4)从铝土矿中提取铝的过程不涉及的化学反应类型是
C
C
;A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(5)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有
CaO、CO2
CaO、CO2
;(6)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系(图2)中正确的是
D
D
.(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号:

①相连的两种物质都是电解质的是
②图中相连的两种物质能够相互反应的是
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为
④用洁净的烧杯取25ml 蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,得到的分散系称为
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼.如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由CO2+Ca(OH)2=CaCO3↓+H20,可完成SO3与NaOH反应的方程式为
②NaHCO3、NaHSO3、NaHS都属于弱酸形成的酸式盐,由NaHCO3+HCl═NaCl+H20+CO2↑及NaHCO3+NaOH═Na2CO3+H20,可完成NaHS分别与HCl、NaOH反应的方程式为
查看习题详情和答案>>

①相连的两种物质都是电解质的是
CD
CD
(填分类标准代号,下同)都是氧化物的是B
B
②图中相连的两种物质能够相互反应的是
D
D
,所属基本反应类型的是复分解
复分解
反应.③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为
Fe2O3+6H+=2Fe3++3H2O
Fe2O3+6H+=2Fe3++3H2O
④用洁净的烧杯取25ml 蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,得到的分散系称为
胶体
胶体
,证明该分散系生成的实验原理是丁达尔效应
丁达尔效应
.(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼.如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由CO2+Ca(OH)2=CaCO3↓+H20,可完成SO3与NaOH反应的方程式为
SO3+2NaOH=Na2SO4+H2O
SO3+2NaOH=Na2SO4+H2O
.②NaHCO3、NaHSO3、NaHS都属于弱酸形成的酸式盐,由NaHCO3+HCl═NaCl+H20+CO2↑及NaHCO3+NaOH═Na2CO3+H20,可完成NaHS分别与HCl、NaOH反应的方程式为
NaHS+HCl=NaCl+H2S↑
NaHS+HCl=NaCl+H2S↑
、NaHS+NaOH=Na2S+H2O
NaHS+NaOH=Na2S+H2O
.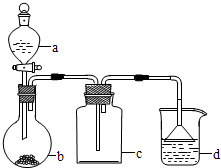 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO2 | H2O |
| D | 饱和食盐水 | CaC2 | C2H2 | KMnO4酸性溶液 |
| A、A | B、B | C、C | D、D |
某食用白醋是由醋酸与纯水配制而成,用0.1000mol/L NaOH溶液准确测定其中醋酸的物质的量浓度.以下为某同学列出的实验步骤(未排序),请回答下列问题.
A.分别向碱式滴定管、酸式滴定管注入NaOH标准溶液和待测醋酸至0刻度以上2~3cm
B.调节滴定管液面至0或0刻度以下,记下读数
C.用NaOH标准溶液滴定至终点,记下滴定管液面的刻度
D.用标准溶液清洗碱式滴定管2~3次;待测醋酸清洗酸式滴定管2~3次
E.用待测醋酸清洗锥形瓶2~3次
F.排气泡使滴定管尖嘴充满溶液,把滴定管固定好
G.滴定管检漏,用水清洗所有仪器,备用
H.通过酸式滴定管向锥形瓶注入20.00mL待测醋酸,并加入2-3滴指示剂
(1)用离子方程式表示该实验的原理
(2)从上述实验步骤中选出正确的并按操作先后排序.你的实验顺序为:(用字母表示)
(3)实验室常用的酸碱指示剂有甲基橙、石蕊和酚酞,你选择的指示剂是
(4)某同学实验后得到的数据如下:
原白醋中醋酸的物质的量浓度为
(5)分析下列操作对测定结果的影响,用“偏低”、“偏高”或“不影响”填空.
①滴定前碱式滴定管充满溶液,滴定后尖嘴处有气泡
②读取标准溶液体积时,滴定前平视,滴定后仰视
查看习题详情和答案>>
A.分别向碱式滴定管、酸式滴定管注入NaOH标准溶液和待测醋酸至0刻度以上2~3cm
B.调节滴定管液面至0或0刻度以下,记下读数
C.用NaOH标准溶液滴定至终点,记下滴定管液面的刻度
D.用标准溶液清洗碱式滴定管2~3次;待测醋酸清洗酸式滴定管2~3次
E.用待测醋酸清洗锥形瓶2~3次
F.排气泡使滴定管尖嘴充满溶液,把滴定管固定好
G.滴定管检漏,用水清洗所有仪器,备用
H.通过酸式滴定管向锥形瓶注入20.00mL待测醋酸,并加入2-3滴指示剂
(1)用离子方程式表示该实验的原理
CH3COOH+OH-=CH3COO-+H2O
CH3COOH+OH-=CH3COO-+H2O
.(2)从上述实验步骤中选出正确的并按操作先后排序.你的实验顺序为:(用字母表示)
G→D→A→F→B→H→C
G→D→A→F→B→H→C
.(3)实验室常用的酸碱指示剂有甲基橙、石蕊和酚酞,你选择的指示剂是
酚酞
酚酞
,理由是两者恰好完全中和生成醋酸钠,其水溶液呈碱性,必需选择在碱性范围变色且颜色容易判断的酚酞作指示剂判断滴定终点
两者恰好完全中和生成醋酸钠,其水溶液呈碱性,必需选择在碱性范围变色且颜色容易判断的酚酞作指示剂判断滴定终点
;滴定终点的现象是当滴加最后一滴氢氧化钠溶液时,溶液变为浅红色且30s不褪色
当滴加最后一滴氢氧化钠溶液时,溶液变为浅红色且30s不褪色
.(4)某同学实验后得到的数据如下:
| 滴定次数 实验数据 |
1 | 2 | 3 | 4 | 5 |
| V(NaOH)/mL(初读数) | 0.00 | 0.20 | 0.00 | 0.10 | 0.05 |
| V(NaOH)/mL(终读数) | 15.75 | 15.20 | 14.98 | 15.12 | 15.05 |
0.07500
0.07500
mol/L(结果保留4位有效数字).(5)分析下列操作对测定结果的影响,用“偏低”、“偏高”或“不影响”填空.
①滴定前碱式滴定管充满溶液,滴定后尖嘴处有气泡
偏低
偏低
;②读取标准溶液体积时,滴定前平视,滴定后仰视
偏高
偏高
.