题目内容
电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料.工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了提取流程图1:
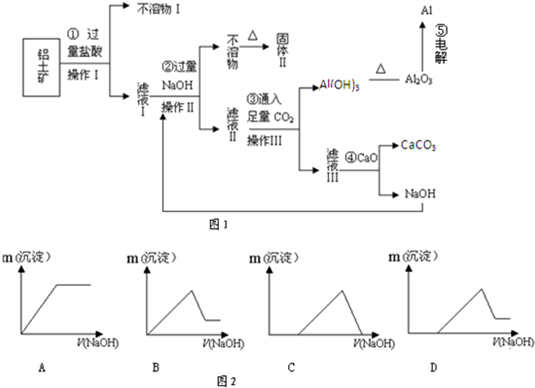
(1)固体Ⅱ的化学式为_
(2)写出流程③的离子方程式
(3)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应
(4)从铝土矿中提取铝的过程不涉及的化学反应类型是
A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(5)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有
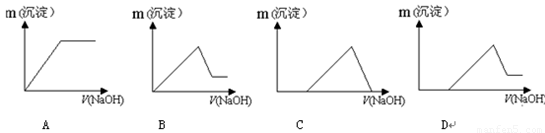
(6)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系(图2)中正确的是

(1)固体Ⅱ的化学式为_
Fe2O3
Fe2O3
,该固体的颜色为红棕色
红棕色
;(2)写出流程③的离子方程式
AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-
AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-
;(3)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应
放出大量的热
放出大量的热
;(4)从铝土矿中提取铝的过程不涉及的化学反应类型是
C
C
;A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(5)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有
CaO、CO2
CaO、CO2
;(6)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系(图2)中正确的是
D
D
.分析:铝土矿可以主要成分为Fe2O3、Al2O3、SiO2,铝土矿加过量盐酸溶解后,Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解,不溶物Ⅰ为SiO2;滤液Ⅰ中含有的阳离子有Fe3+、Al3+、H+,加入过量烧碱,氢离子和氢氧化钠反应生成水,铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,过滤所得出的为Fe(OH)3,滤液Ⅱ含有AlO2-、Cl-、OH-,通入过量二氧化碳气体,得到Al(OH)3沉淀,加热分解生成Al2O3,电解可得到铝;滤液Ⅲ含有碳酸氢根离子,加入氧化钙可生成碳酸钙和氢氧化钠,其中氢氧化钠可循环使用,结合物质的性质以及题目要求可解答该题.
解答:解:铝土矿可以主要成分为Fe2O3、Al2O3、SiO2,铝土矿加过量盐酸溶解后,Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解,不溶物Ⅰ为SiO2;滤液Ⅰ中含有的阳离子有Fe3+、Al3+、H+,加入过量烧碱,氢离子和氢氧化钠反应生成水,铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,过滤所得出的为Fe(OH)3,滤液Ⅱ含有AlO2-、Cl-、OH-,通入过量二氧化碳气体,得到Al(OH)3沉淀,加热分解生成Al2O3,电解可得到铝;滤液Ⅲ含有碳酸氢根离子,加入氧化钙可生成碳酸钙和氢氧化钠,其中氢氧化钠可循环使用,
(1)滤液Ⅰ中含有的阳离子有Fe3+、Al3+、H+,加入过量烧碱生成Fe(OH)3,加热分解生成Fe2O3,颜色为红棕色,故答案为:Fe2O3;红棕色;
(2)滤液Ⅱ含有AlO2-、Cl-、OH-,通入过量二氧化碳气体,得到Al(OH)3沉淀,反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,
故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(3)铝热反应放出大量的热,常用于冶炼熔点高、难熔化的金属的冶炼,铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应放出大量的热,
故答案为:放出大量的热;
(4)反应①②③④为复分解反应,反应⑤为氧化还原反应,氢氧化铁、氢氧化铝生成氧化物的反应为分解反应,不涉及置换反应,故答案为:C;
(5)根据反应流程可知,反应需要NaOH、水、二氧化碳以及氧化钙等物质为原料,生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有CaO、CO2,其中氧化钙可由碳酸钙加热分解制得,
故答案为:CaO; CO2;
(6)滤液Ⅰ中含有的阳离子有Fe3+、Al3+、H+,加入过量烧碱,氢离子和氢氧化钠反应生成水,铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,则符合的图象为D,故答案为:D.
(1)滤液Ⅰ中含有的阳离子有Fe3+、Al3+、H+,加入过量烧碱生成Fe(OH)3,加热分解生成Fe2O3,颜色为红棕色,故答案为:Fe2O3;红棕色;
(2)滤液Ⅱ含有AlO2-、Cl-、OH-,通入过量二氧化碳气体,得到Al(OH)3沉淀,反应的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,
故答案为:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-;
(3)铝热反应放出大量的热,常用于冶炼熔点高、难熔化的金属的冶炼,铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应放出大量的热,
故答案为:放出大量的热;
(4)反应①②③④为复分解反应,反应⑤为氧化还原反应,氢氧化铁、氢氧化铝生成氧化物的反应为分解反应,不涉及置换反应,故答案为:C;
(5)根据反应流程可知,反应需要NaOH、水、二氧化碳以及氧化钙等物质为原料,生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有CaO、CO2,其中氧化钙可由碳酸钙加热分解制得,
故答案为:CaO; CO2;
(6)滤液Ⅰ中含有的阳离子有Fe3+、Al3+、H+,加入过量烧碱,氢离子和氢氧化钠反应生成水,铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,则符合的图象为D,故答案为:D.
点评:本题以框图题形式考查铝的化合物的性质,侧重于学生的分析能力和实验能力的考查,清楚冶炼铝工艺流程原理,熟练掌握“铝三角”的相关反应是解答的关键,题目难度中等.

练习册系列答案
相关题目
(12分)电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料。工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了如下提取流程图

|
|
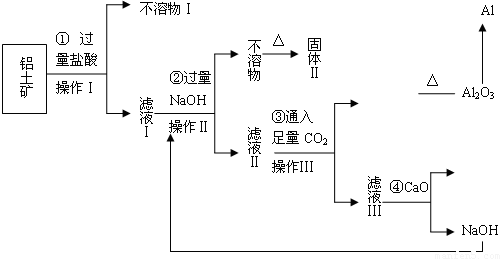
(1)固体Ⅱ的化学式为_ ▲ ,该固体的颜色为 ▲ ;
(2)在实际工业生产流程⑤中需加入冰晶石,目的是 ▲ ;
(3)写出流程③的离子方程式 ▲ ;
(4)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应 ▲ ;
(5)从铝土矿中提取铝的过程不涉及的化学反应类型是 ▲ ;
A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(6)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有_ ▲ _;
(7)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是